实验性药物开发方法为耐药性白血病提供更好的靶向疗法
约翰霍普金斯金梅尔癌症中心研究人员的新研究表明,为什么临床试验中用于治疗某种形式的急性髓性白血病 (AML) 的一些药物经常失败,并展示了一种恢复其有效性的方法。
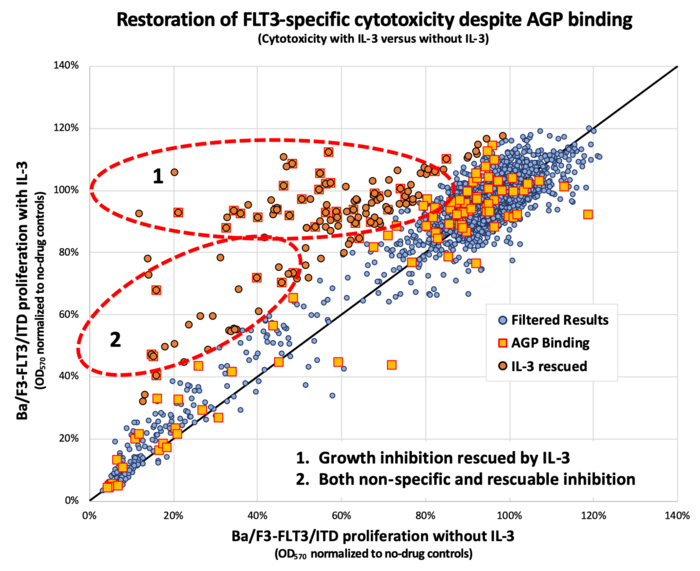
这项临床前研究于 9 月发表在Blood Cancer Discovery 上,可能清除了开发 AML 分子靶向疗法的药理学障碍。
大约三分之一的 AML 患者在基因 FLT3 中有突变。正常的 FLT3 基因会产生一种酶,向骨髓干细胞发出生长和补充信号。当发生突变时,FLT3 会导致白血病细胞快速生长,从而导致治疗后更高的复发率和更低的总体存活率。
FLT3 突变的 AML 对一类称为 e 家族酪氨酸激酶抑制剂 (TKIs) 的药物特别敏感,使它们成为药物开发的主要候选者,第一作者 David Young 医学博士说,他在约翰霍普金斯金梅尔癌症中心。Young 博士现在在美国国立卫生研究院的国立心肺血液研究所工作。
然而,这些 TKI 和其他药物经常失败并且患者会复发。在对人类白血病细胞系和小鼠进行的一系列实验中,Kimmel 癌症中心团队证明人类 α(1)-酸性糖蛋白 (AGP) 与药物结合,有效阻止其达到预期的 FLT3 突变目标并杀死癌症细胞。
Donald Small,医学博士,博士约翰霍普金斯金梅尔癌症中心儿科肿瘤学部主任、Kyle Haydock 肿瘤学教授和同事用来他替尼、TTT-3002 或midostaurin a美国食品和药物管理局 (FDA) 批准的针对不同浓度的 FLT3 的药物。血浆是血液中含有蛋白质和其他非细胞因子的透明部分。他们发现,与其他来源的血液成分不同,添加人血浆会降低 TKI 抑制 FLT3 的能力。进一步的测试确定人类 AGP 与这三种药物结合并抑制它们杀死白血病细胞的能力。
为了证明这些发现的临床相关性,研究人员从新诊断出患有 AML 的成年人身上收集了血液样本,并研究了他们的血浆对米多林的影响。在存在高度炎症的情况下,例如在新诊断的白血病患者中,AGP 水平会升高。正如预期的那样,药物在这些病例的人血浆分析中失去了效力。
“Midostaurin 非常具体且有效,自 2017 年 FDA 批准其用于成人 AML 以来,我们已经看到患者预后改善了约 10%,”Young 说,“但我们从未获得过‘本垒打’。寻找,因为它受 AGP 约束。”
在另一组实验中,该团队表明,这种血浆蛋白抑制可以通过添加一种也与 AGP 结合的试剂来逆转。已知米非司酮与 AGP 的结合亲和力与研究中的三种药物相当或更高。研究人员用人血浆蛋白、米司他林和米非司酮进行了 FLT3 检测。他们发现米非司酮取代了 AGP 结合的midostaurin,恢复了其抗FLT3活性。在老鼠身上测试这个概念,他们得到了相似的结果。