前列腺癌转移新调节因子的发现
一种通常与前列腺癌中雄激素受体活性相关的转录因子,最近被发现在控制脂质生物合成方面发挥作用,这是西北医学发表在《Nature Genetics》杂志上的一项研究成果。
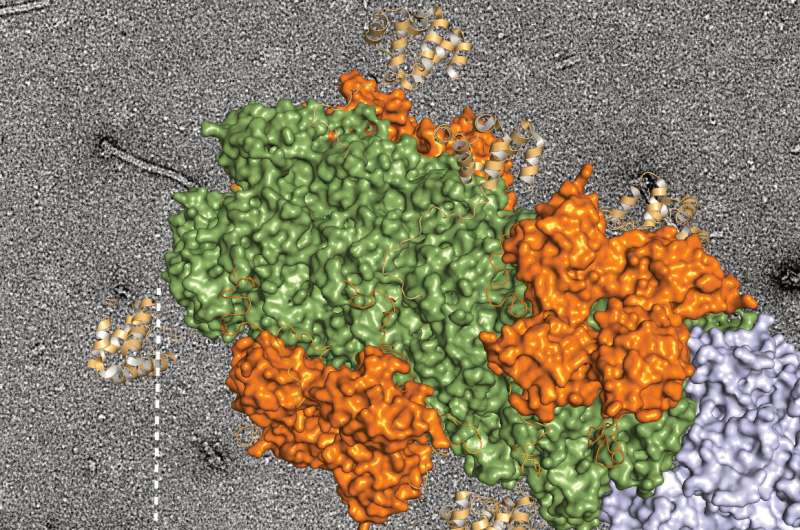
该研究的资深作者、血液学和肿瘤学学部医学教授、医学博士Jindan Yu表示,被称为HOXB13的转录因子在晚期前列腺癌中被下调,释放脂质生物合成并加速癌症转移。
“HOXB13主要研究基因激活,但我们的研究显示其主要功能在脂质合成的转录镇压,”Yu说。
HOXB13是一种前列腺特异性蛋白,在前列腺发育过程中高度表达。它能增强雄激素受体(AR)功能,从而帮助前列腺细胞生长。
在前列腺癌,雄激素燃料不受控制的细胞生长和AR抑制剂治疗是主要的护理。然而,大多数转移性前列腺癌最终会对AR疗法产生耐药性,肿瘤最终会变得更像干细胞,从而减少对雄激素的依赖。既往研究表明,HOXB13与AR有显著的相互作用,但二者的表达模式并不匹配,随着癌症的进展,HOXB13下调而AR上调。
Yu说:“我们认为HOXB13缺失了一些东西,因为HOXB13和AR表达发生了分歧。”
在目前的研究中,科学家研究了HOXB13的非AR功能,发现转录因子在抑制脂质生物合成方面有一个完全独立的功能,作为人体正常防御癌症的一部分。然而,随着前列腺癌细胞失去谱系并产生治疗耐药性,它们也失去了前列腺特异性HOXB13的表达,从而导致可促进癌症转移的脂质生物合成的显著增加。
“这些细胞忘记了自己是谁,这使它们对AR抑制剂具有抵抗力,并有助于癌症扩散,”Yu说。
超过30%的治疗难治性前列腺癌患者hoxb13是阴性的,因此他们的肿瘤中脂质生物合成升高,因此靶向这一途径可能有助于延长晚期前列腺癌患者的生存期。
一种名为TVB-2640的药物已经在乳腺癌和小细胞肺癌的临床试验中,可能会有所帮助:这种药物抑制一种对脂质生物合成途径至关重要的酶,恢复一些正常的抑制作用,这种抑制作用是对细胞增殖和癌症的自然防御。
“现在,我们只需要确定使用这种药物的最佳人群,”于说。
这项研究还帮助解释了G84E的奇怪情况,HOXB13的家族突变增加了早发前列腺癌的风险,但G84E突变患者和非患者的癌症严重程度没有区别。这种疾病的发病机制此前未知,但目前的研究发现,这种突变破坏了脂质生物合成抑制,增加了前列腺特异性抗原(pSA)的水平,pSA是一种有时被用于筛查前列腺癌的生物标志物。
Yu和合著者William Catalona医学博士说,这些发现增加了一种可能性,即观察到的与G84E相关的早发性前列腺癌风险的增加可能是流行病学的诡计,而不是诊断时真正的致病突变。他是泌尿学教授,也是使用pSA作为前列腺癌筛查工具的先驱。
“这些患者有家族史,所以他们经常在更年轻的时候进行前列腺癌筛查,”Yu说。“对G84E患者的早期诊断确保了在早期阶段对疾病进行管理,这可能在G84E变得具有致病性并促进肿瘤转移之前治愈疾病,从而提供保护。”
由西北大学提供