科学家发现两种修复肿瘤血管的新方法
肿瘤发出的信号会损害正常的血液流动,这使得各种类型的癌症治疗,包括放疗、化疗、靶向治疗和免疫治疗,都难以对其进行治疗。血液供应受损会造成低氧环境,即缺氧,导致肿瘤具有侵袭性特征,并受到免疫抑制。为了应对这一挑战,由麻省总医院(MGH)的研究人员领导的团队开发了两种方法来修复肿瘤血管并改善其功能。同时,通过设计一个方法来评估这些方法的效果和测试它在临床癌症研究发表的一项研究中,美国癌症研究协会杂志》上,研究人员发现,每种方法可能有助于恢复血流增强化疗的癌症细胞,缓解缺氧,把它们结合起来可能特别有效。
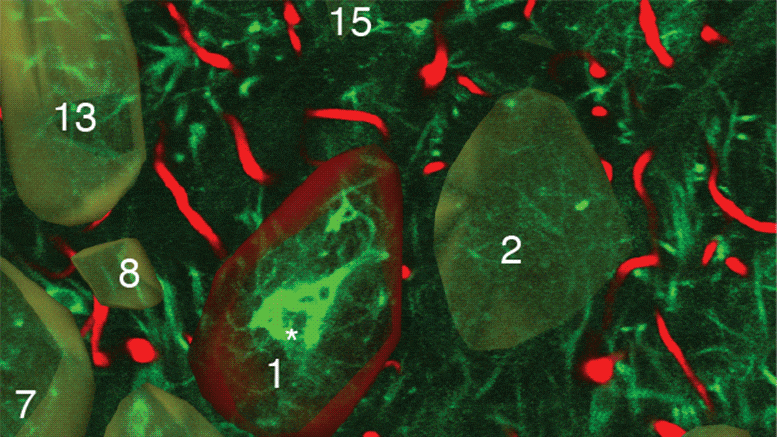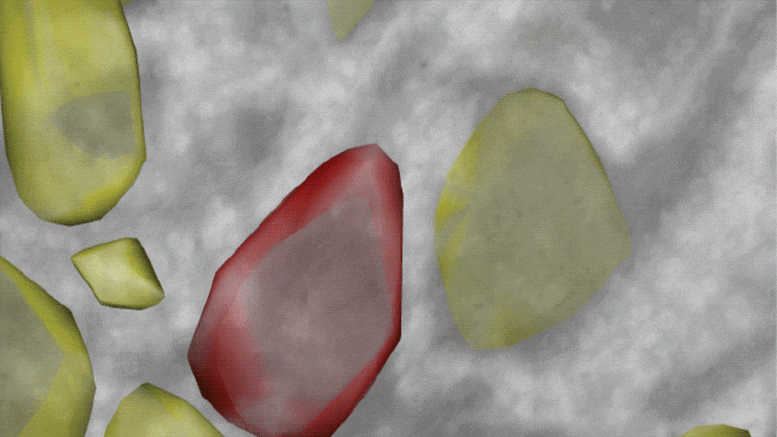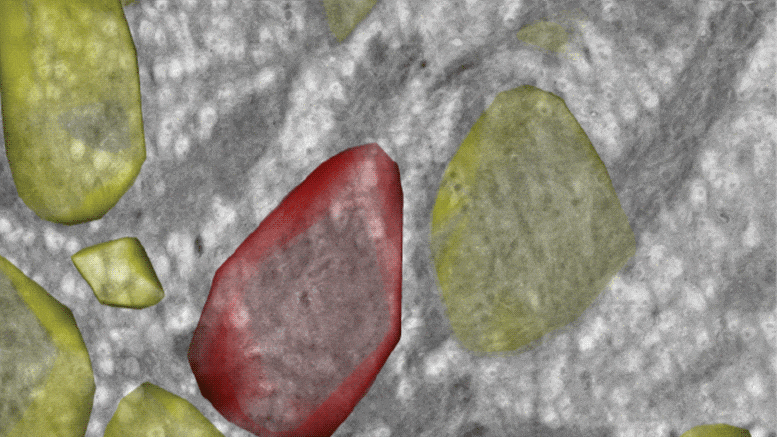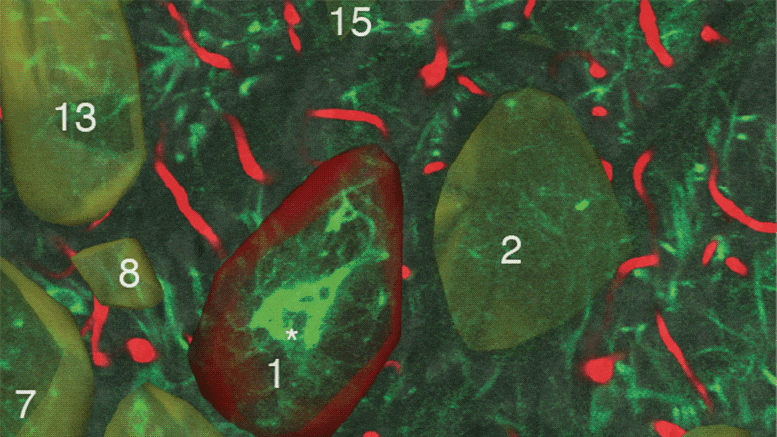
科学家们的评估方法包括测量氧含量,作为肿瘤内缺氧和异常血流程度的指标。“这项研究报告了一种具有独特特性的新型显微镜系统的开发和应用,”资深作者Rakesh K. Jain博士说,他是MGH肿瘤生物学E.L. Steele实验室的主任,也是哈佛医学院放射肿瘤学的Andrew Werk Cook教授。“首先,该系统能够成像细胞内的氧浓度,以及与携带氧的血管相关的大量肿瘤组织。其次,该系统可以随时间成像肿瘤组织中的氧浓度,以便观察治疗期间氧合的变化。”
Jain和他的同事们使用他们的显微镜系统来检查他们修复肿瘤血管异常减少血液流动的两种方法的效果:一种使用抗血管生成疗法,靶向影响血管形成的途径,另一种涉及所谓的血管紧张素系统抑制剂,它可以减轻肿瘤生长产生的压垮肿瘤血管的压力。氯沙坦是一种被批准用于治疗高血压的药物,是一种血管紧张素系统抑制剂。
“我们的显微镜分析显示,尽管每种方法都能缓解肿瘤的缺氧,但效果是混合的例如,根据肿瘤类型和剂量有不同的结果,”合著者John D. Martin博士说,他在这项研究期间是斯蒂尔实验室的博士生,现在是东京纳米载体有限公司的研究科学家。这两种方法引起的互补的血管变化表明,将它们结合起来有可能产生更强大的效果。
“理解肿瘤缺氧,抗血管新生疗法和洛沙坦影响缺氧——如何影响疾病进展和治疗抵抗,”瑞安说,该研究陈年,医学博士,博士,他是一个博士生在斯蒂尔实验室研究助理教授,现在是科罗拉多大学的医学院。“在肺、肾、肝和子宫内膜癌的特定情况下,抗血管生成疗法与化疗和免疫疗法相结合,被用作护理标准。同样,在MGH合作者领导的多机构临床试验中,氯沙坦正在进行化疗和免疫治疗胰腺癌的临床研究。”
文章标题Multiphoton phosphorescence quenching microscopy reveals kinetics of tumor oxygenation during anti-angiogenesis and angiotensin signaling inhibition