终于发现让人不再暴饮暴食的方法!科学家找到大脑中控制食物摄入的信号通路
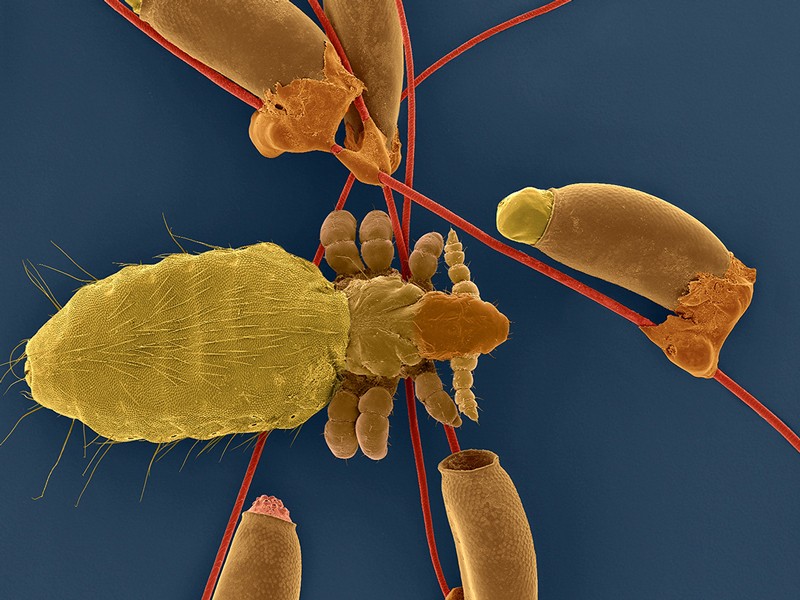
图片:小鼠大脑的神经细胞(绿色)和蛋白质pRG-1(红色)。如果神经细胞含有pRG-1,细胞就会呈现黄色。
一组研究人员开发了一种治疗饮食失调的全新方法。科学家们证明,下丘脑中的一组神经细胞(所谓的AgRp,豚鼠相关肽神经元)控制内源性溶血磷脂的释放,而溶血磷脂反过来控制大脑皮层神经细胞的兴奋性,从而刺激食物摄入。在这一过程中,信号通路的关键步骤由自体taxin酶控制,它负责在大脑中产生溶血磷脂酸(LpA),作为网络活动的调节器。因此,在动物模型中,给予自体taxin抑制剂可以显著减少空腹后的过量进食和肥胖。
饮食失调,尤其是肥胖,是世界各地工业化社会各种疾病的最常见原因之一,特别是具有永久性残疾或致命后果的心血管疾病,如心脏病发作、糖尿病或中风。罗伯特·科赫研究所(Robert Koch Institute)在2021年报告称,德国有67%的男性和53%的女性超重。23%的成年人严重超重(肥胖)。迄今为止,用药物来影响饮食行为的尝试被证明是无效的。一种调节控制饮食行为的神经网络兴奋性的新疗法,将是控制这种普遍肥胖的决定性一步。
研究小组发现,在突触LpA信号受损的人群中,肥胖和随之而来的II型糖尿病的发病率增加。由Johannes Vogt教授(科隆大学医学院)、Robert Nitsch教授(Münster大学医学院)和Thomas Horvath教授(美国纽黑文耶鲁医学院)领导的研究小组现在已经表明,LpA控制大脑皮层神经元的兴奋性在控制进食行为中起着至关重要的作用:AgRp神经元调节血液中溶磷脂酰胆碱(LpC)的数量。通过主动运输,LpC到达大脑,在那里它被autotaxin (ATX)酶转化为LpA,在突触上活跃。突触LpA信号刺激大脑中的特定网络,从而导致食物摄入的增加。
在小鼠模型中,禁食一段时间后,血液中LpC的增加导致了大脑中LpA刺激的增加。这些小鼠表现出典型的觅食行为。两者均可通过给予自体taxin抑制剂实现规范化。另一方面,肥胖的小鼠在连续服用这些抑制剂后体重下降。
Vogt解释说:“我们发现,通过基因突变和ATX的药理抑制,过量食物摄入和肥胖的人数显著减少。因此,我们多年来研究的关于脑内多巴胺控制的兴奋性的基本发现,也在饮食行为中发挥着核心作用。”
Nitsch认为这一发现是新药研发的重要一步:“数据显示,突触LpA信号通路紊乱的人更有可能超重和患二型糖尿病。”这是ATX抑制剂治疗成功的有力迹象,我们目前正在与位于耶拿的Hans Kn?ll研究所共同开发用于人类的ATX抑制剂。”
这些关于神经元网络在进食行为中通过溶血磷脂的兴奋控制的发现,以及他们提出的新的治疗可能性,在未来不仅有助于治疗饮食失调,还有助于治疗神经和精神疾病。
文章标题AgRp neurons control feeding behaviour at cortical synapses via peripherally derived lysophospholipids