这种微小的基因片段在视网膜发育和视力中扮演着至关重要的新角色
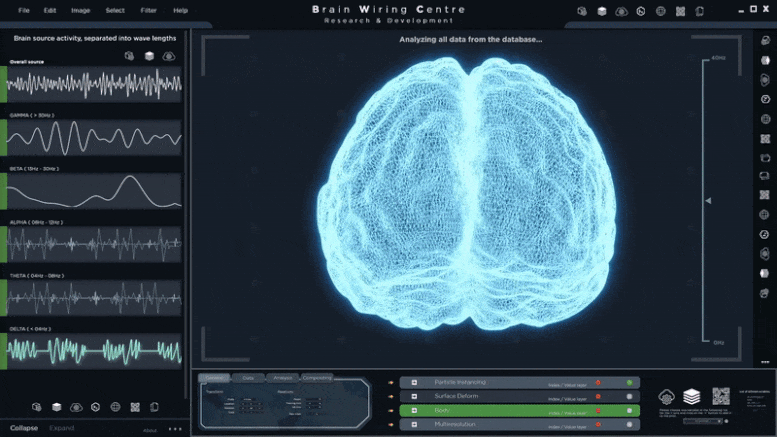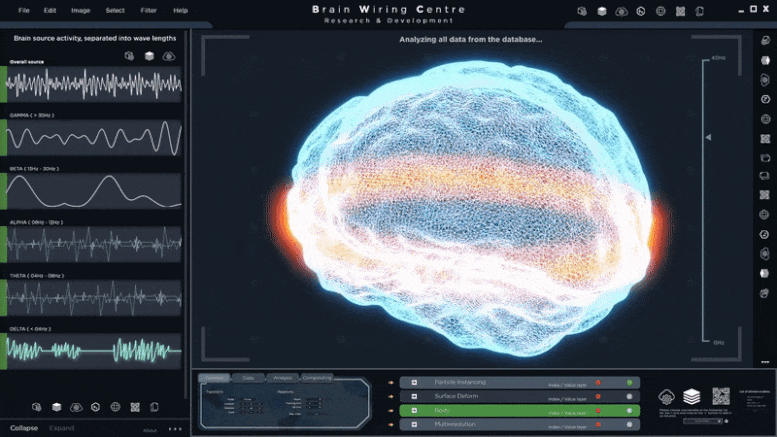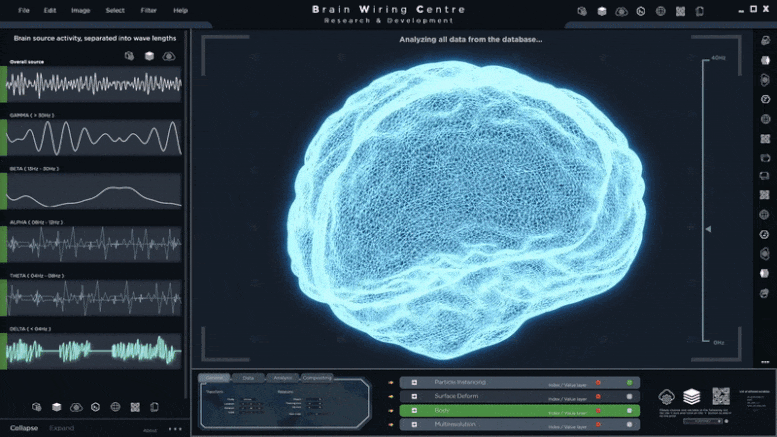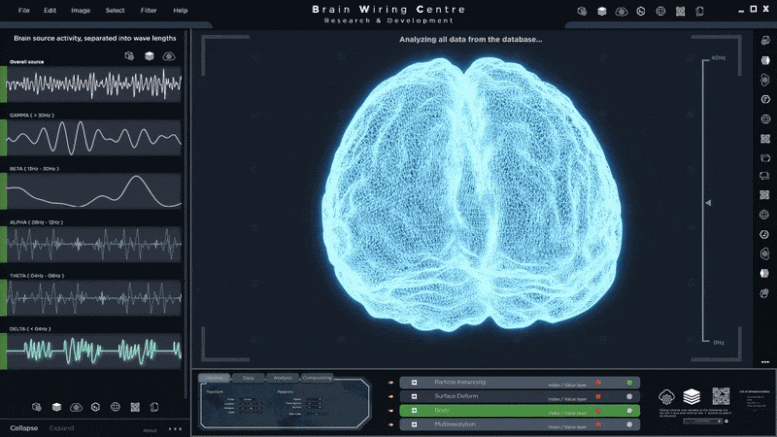
斑马鱼的视网膜细胞的外节,部分感光细胞负责将光转化为神经信号,使视觉,在图像的顶部被染成绿色。与正常视网膜细胞(左)相比,Srrm3基因被敲除的视网膜细胞(右)的外节明显降解。
巴塞罗那基因组调控中心(CRG)的研究人员揭示了Srrm3是一个对光感受器发育至关重要的主调节基因,光感受器是视网膜后部的细胞,它捕捉和处理光线,向大脑发送信号,使视觉得以实现。在斑马鱼中敲除这种基因会导致严重的视觉损伤。
研究发现,在脊椎动物中,Srrm3通过调节可变剪接而起作用,可变剪接是一种允许细胞从一个基因中产生多种蛋白质的过程,在神经元细胞中尤为突出。选择性剪接的错误调控可能会对人类健康造成毁灭性的影响,例如癌症或神经系统疾病。
Srrm3发现它能特别调控微外显子的剪接,微外显子是DNA中只有3-27个字母长的微小片段。尽管微外显子的尺寸很小,但其调控在蛋白质和细胞功能中发挥着关键作用。
研究人员发现了几十种不同的微外显子,这些微外显子主要存在于光感受器中,而不存在于其他神经元中。这些微外显子的很大一部分影响着大约70个基因的功能,这些基因对感光器外段的发育很重要,感光器外段是细胞吸收光线的部分。研究结果发表在《pNAS》。
这项研究揭示了视网膜细胞独特的细胞形状和功能所需要的一种新的细胞专门化层,视网膜细胞是人体中最复杂和专门化的细胞之一。由于这种复杂性,视网膜细胞的发育依赖于许多独特的基因,其中任何一种都可能产生致病突变并导致视力丧失。
遗传性视力丧失最常见的原因之一是色素性视网膜炎,这是一种涉及分子机制的遗传疾病。40%到50%的色素性视网膜炎病例无法解释,这意味着它们携带的基因突变尚未被发现。该研究的作者计划开展未来的研究来评估是否Srrm3或者,所涉及的微外显子可以解释其中一些案例。
“Srrm3基因与感光细胞的发育和视网膜疾病的发病机制都没有关系。我们已经在探索这种基因在没有基因诊断的病人中的作用。如果我们发现这种特定基因或任何视网膜微外显子发生突变的病例,这可能会导致管理这种疾病的潜在新治疗策略,”文章第一作者Ludovica Ciampi博士说。
ICREA研究教授Manuel Irimia表示,理解特定细胞类型的微外显子调控是识别新的治疗靶点的关键。“由于可选择性剪接和微外显子的调节,光感受器具有独特的特性。这有助于使细胞更专门化,但也可能更容易受到遗传疾病的影响。调节剪接活动现在是可能的,所以我们揭示的生物学越复杂,我们就越有可能找到治疗视网膜疾病的治疗靶点,”Irimia博士总结道。
这项研究是ICREA研究教授Luis Serrano和CRG的Manuel Irimia,以及意大利那不勒斯Telethon遗传与医学研究所和瑞士苏黎世大学合作的结果。这项工作由欧洲研究理事会、西班牙科学与创新部和加泰罗尼亚委员会资助。
Specialization of the photoreceptor transcriptome by Srrm3-dependent microexons is required for outer segment maintenance and vision