曾艺组建立基于Procr干细胞的体外长期扩增胰岛类器官的新方法
北京时间4月8日,国际著名学术期刊 Nature protocols 在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)曾艺研究组的最新文章 “Isolation of mouse pancreatic islet procr+ progenitors and long-term expansion of islet organoids in vitro”。该研究工作建立了分离小鼠胰岛中 procr 干细胞并在体外长期扩增小鼠胰岛类器官的技术方法。
近年来,胰岛移植作为新兴的糖尿病治疗方法,在临床应用上取得了一定的成功,但供体胰岛的严重不足极大地限制了这种治疗手段的进一步普及。因此,发展在体外产生大量表达胰岛素的β细胞的技术方法具有巨大的临床应用价值。此前的方法主要有两种,第一种是基于胚胎干细胞 (ESCs) 和诱导性多能干细胞 (ipSCs) 的定向诱导分化获取功能性胰岛细胞。这类研究较广泛地在国际多个实验室开展,已经取得了卓越的进展。然而,这类方法仍需要体外多步骤诱导分化,工艺复杂、时程长,其中混杂的未能完全分化的细胞具有成瘤隐患。第二种是以胰腺组织的细胞为来源,从胰腺导管细胞 (Duct cells) 或胰岛α细胞转分化产生β细胞,但现阶段这类方法效率很低,不能大量产生β细胞。科研人员认为,以胰岛的成体干细胞为来源,在体外制备功能性胰岛类器官,理论上是更安全的、分化途径最短、工艺最简单的获得β细胞的方法。而且,β细胞的功能(响应糖刺激、分泌胰岛素)需要胰岛内其它各类内分泌细胞(α,delta, pp)的相互作用,从成体干细胞为来源的胰岛类器官正是包含胰岛所有的内分泌细胞类型,展现出这类方法获得的“人工胰岛”的功能的卓越性。
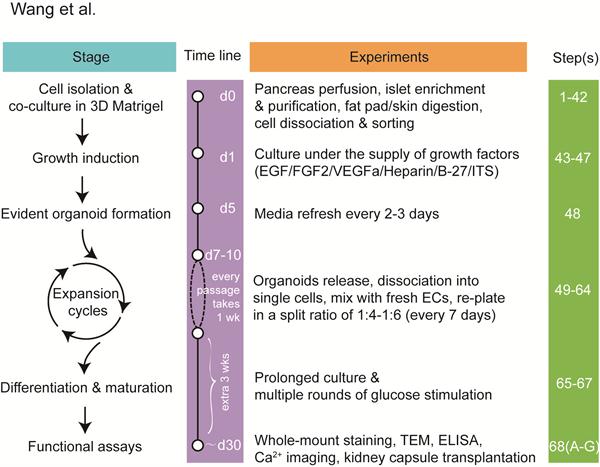
曾艺研究组长期致力于成体干细胞的研究,包括鉴定干细胞身份属性、确定干细胞信号调控机制、研究干细胞与疾病的关系以及建立基于干细胞的体外类器官培养体系等。2020年发表的Cell文章中发现并鉴定了小鼠胰岛成体干细胞,并建立了小鼠胰岛类器官体外长期扩增的培养体系。本次的研究工作详细分解了小鼠胰岛类器官培养的技术方法。首先描述了如何从小鼠中分离procr胰岛干细胞,接着通过干细胞与血管内皮细胞的共培养方法,建立了体外高效形成可长期扩增的胰岛类器官的体系,可使这类胰岛类器官达到成熟状态,最后提供了体外、体内评估胰岛类器官成熟程度和功能有效性的多个下游试验方法。该研究为体外长期培养并获得大量功能性小鼠胰岛β细胞贡献了详细的技术方法,也为体外获得大量人胰岛β细胞提供了重要的提示。
分子细胞卓越中心王经强博士、王代松博士为该研究论文的共同第一作者。该论文的其他作者包括曾艺研究组白蓝月博士、博士研究生陈心怡、苑舒博、刘春业。特别感谢分子细胞卓越中心细胞分析技术平台、中国科学院上海营养与健康研究所生物医学大数据中心的大力支持。该项成果获得中科院先导项目、科技部项目、国家自然科学基金委等的经费支持。
文章链接:https://doi.org/10.1038/s41596-022-00683-w