基础医学院童雪梅研究员团队发现结直肠癌微环境Treg细胞代谢调控新机制
2021年4月23日,上海交通大学基础医学院生化与分子细胞生物学系童雪梅研究员课题组、上海市免疫学研究所李斌研究员课题组和上海交通大学医学院附属新华医院陈寒蓓主任医师等合作在Gastroenterology杂志在线发表题为MondoA-TXNIp axis maintains regulatory T cell identity and function in colorectal cancer microenvironment的研究论文,揭示MondoA-TXNIp调控结直肠癌微环境Treg细胞代谢模式和功能的新作用。

结直肠癌是全球发生率第二、死亡率第三的恶性肿瘤。调节性T细胞(Treg)是一类免疫负向调控细胞,在结直肠肿瘤微环境中高度浸润,是构成免疫抑制微环境的主要细胞亚群之一,因此作为肿瘤免疫治疗的重要靶标受到广泛关注。结直肠癌浸润Treg细胞感应低氧、营养物质缺乏、酸性环境等多重压力,呈现出代谢模式和生理功能的高度异质性,然而,肿瘤微环境代谢信号如何影响结直肠癌浸润Treg群体的异质性仍有待阐明。
童雪梅研究团队通过分析单细胞测序数据,发现结直肠癌浸润Treg细胞糖酵解活性增强,深入探究发现结直肠癌浸润Treg细胞下调MondoA-TXNIp转录调控轴功能,增加葡萄糖转运蛋白Glut1表达和细胞膜定位,诱导高糖酵解代谢模式下的Th17-like Treg细胞,削弱其免疫抑制功能,进一步促进Th17型炎症,抑制CD8+T细胞的抗肿瘤功能,并最终促进结直肠癌发生发展(图1)。
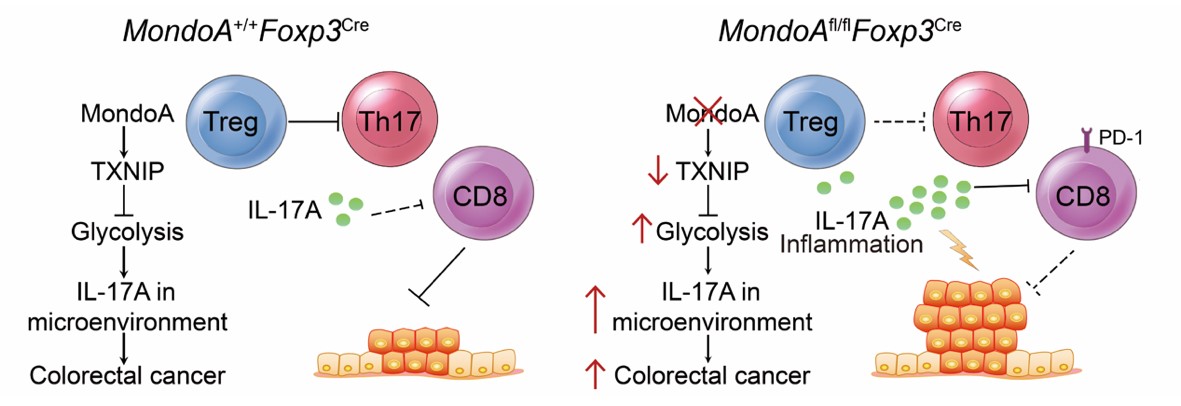
图1MondoA-TXNIp调控结直肠癌微环境Treg细胞代谢、功能和肿瘤进程。
结直肠癌免疫检查点抑制剂疗法在错配修复缺陷的微卫星不稳定性亚型患者中显示出较好的疗效,而占据结直肠癌病人80-90%的微卫星稳定性亚型患者对于肿瘤免疫治疗几乎不响应,已有报道显示微卫星稳定性的结直肠癌中Th17细胞大量富集。童雪梅团队这项工作证实靶向IL-17A的anti-IL17A抗体治疗能显著抑制结直肠癌发生发展,并且anti-IL-17A抗体联合anti-pD-1抗体治疗效果更佳。研究团队创新性地探索了靶向炎症的中和抗体和免疫检查点抑制剂联合治疗结直肠癌的的新方案,为微卫星稳定性亚型的结直肠癌病人从肿瘤免疫治疗中获益提供了可能的新干预靶点。该项研究得到MondoA基因发现者、美国犹他大学Don Ayer教授的来信祝贺和高度评价。
上海交通大学基础医学院博士后卢颖、上海市免疫学研究所博士后李扬扬为该研究论文的共同第一作者,此项研究得到上海交通大学医学院附属新华医院、复旦大学附属肿瘤医院等单位的大力协助,通讯作者为童雪梅研究员、李斌研究员和陈寒蓓主任医师。该研究工作获得了上海市科学技术委员会科学基金委、国家自然科学基金委、国家重点研发计划等资助。
相关论文信息:https://doi.org/10.1053/j.gastro.2021.04.041






























