我国科研人员揭示心肌细胞钙信号和兴奋收缩耦联的分子调控原理
在国家自然科学基金项目(批准号:91854209、31630035)的资助下,北京大学王世强教授实验室揭示了冬眠动物赖以增强其兴奋收缩耦联效率的钙信号相关蛋白转录调控机制,提出了心肌细胞钙信号和兴奋收缩耦联分子调控的基本原理。相关成果以“冬眠黄鼠心肌细胞中钙信号的分子转录调控机制:“心肌蛋白-亲联蛋白”信号轴(Transcriptional regulation of intermolecular Ca2+ signaling in hibernating ground squirrel cardiomyocytes: The myocardin–junctophilin axis)”为题,于2021年4月6日发表在著名学术期刊《美国科学院院报》(proc Natl Acad Sci USA)。论文链接:https://doi.org/10.1073/pnas.2025333118。
冬眠是多种小型哺乳类、鸟类动物适应寒冷缺食的冬季演化产生的节能行为。冬眠动物的心脏在深低体温下虽然心率减慢,但收缩愈发有力。因此,阐明冬眠动物兴奋收缩耦联钙信号的调控原理,并应用于心力衰竭的防治策略研究,具有重要的研究意义和研究价值。而心肌细胞中横管膜与肌质网膜是平行排列的,二者之间的钙信号转导决定着心脏的收缩能力。王世强教授实验室克服了非模式动物研究的诸多制约因素,采用多种研究手段进行深入探索,提出了“MyoCD-JpH2调控轴”的系统理论。其中,心肌特异性转录因子MyoCD通过SRF促进JpH2和CAV3基因的“协奏转录”。而JpH2和CAV3是一对互作蛋白,分别定位于肌质网与横管膜,二者虽然分子序列迥异,但都具有相似的类CArG顺式作用元件,可以共用MyoCD-SRF转录机器。JpH2和CAV3之间的协奏转录促进二者之间的相互作用,有利于形成肌质网与横管膜之间的纳米耦联结构,从而压缩横管钙通道与肌质网钙释放通道间的物理空间,进而提高兴奋收缩耦联的分子效率(图1)。这一“协奏转录”新原理为保证互作蛋白的化学配比提供了优化方案。
王世强教授实验室提出的“协奏转录”和“MyoCD-JpH2调控轴”等新概念、新理论不仅揭示了冬眠动物耐低体温生存的关键适应性机制,提出了冬眠动物作为“反心衰模型”的研究价值,同时代表了心肌细胞钙信号和兴奋收缩耦联调控的一般原理,为相关心脏疾病的研究提供了新思路。
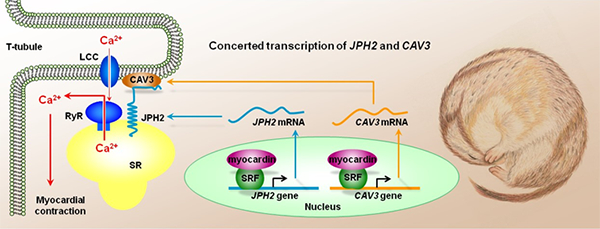
图1 心肌细胞横管膜与肌质网膜钙信号转导的分子调控机制






























