【文献解读】华中科技大学发现骨髓瘤骨病的新型标志物
这篇题为“Tumor-derived extracellular vesicles inhibit osteogenesis and exacerbate myeloma bone disease”的文章于1月发表在《Theranostics》杂志(IF: 8.537)上。华中科技大学同济医学院附属协和医院的李秋柏教授和生命科学与技术学院的郭安源教授为共同通讯作者。
背景介绍
在我国,多发性骨髓瘤(MM)的发病率已超过急性白血病,位居血液系统恶性肿瘤的第二位。大约80%的患者会出现骨髓瘤骨病(MBD),严重影响了患者的生活质量及生存期。MBD的特点在于成骨细胞活性严重受损,这是因为骨髓来源的间充质干细胞(BM-MSC)成骨功能受阻。不过,受阻的具体机制还不太清楚。
最近,越来越多的证据表明,细胞外囊泡(EV)是以往被忽略的细胞间通讯机制。癌细胞会释放含有多种分子的细胞外囊泡,如蛋白质、RNA和miRNA,影响肿瘤微环境。于是,研究人员此次研究了骨髓瘤细胞外囊泡(MM-EV)的生物活性成分,并检测了它对BM-MSC成骨功能以及骨髓瘤骨病的影响。
MM-EV富含调节MBD的各种分子
研究人员从人多发性骨髓瘤细胞系RpMI 8226和U266中分离出MM-EV,分别称之为R-EV和U-EV。这些EV为球形,大小在200-1000 nm。它们是CD138、Annexin-V和pKH-26阳性的,同时表达EV标志物Alix、TSG101、CD63、MFGE8或CD9。
之后,他们对R-EV中的RNA分子进行测序。由于miRNA被选择性分泌到EV中,并充当主要调节因子,他们重点分析了R-EV中包含的miRNA,并与来自B细胞和K562白血病细胞的EV进行比较。R-EV表达了287种miRNA,而K562-EV表达176种miRNA。
他们发现,一些调节细胞增殖的miRNA在R-EV和K562-EV中高表达。有意思的是,一些参与成骨细胞或破骨细胞分化的miRNA只在R-EV中高表达,如miR-103a-3p、miR-181a-3p和miR-21-3p。这些结果表明,R-EV所包含的miRNA不仅在细胞增殖中发挥作用,还与骨髓瘤骨病的发展相关。
MM-EV在体外抑制BM-MSC的成骨功能
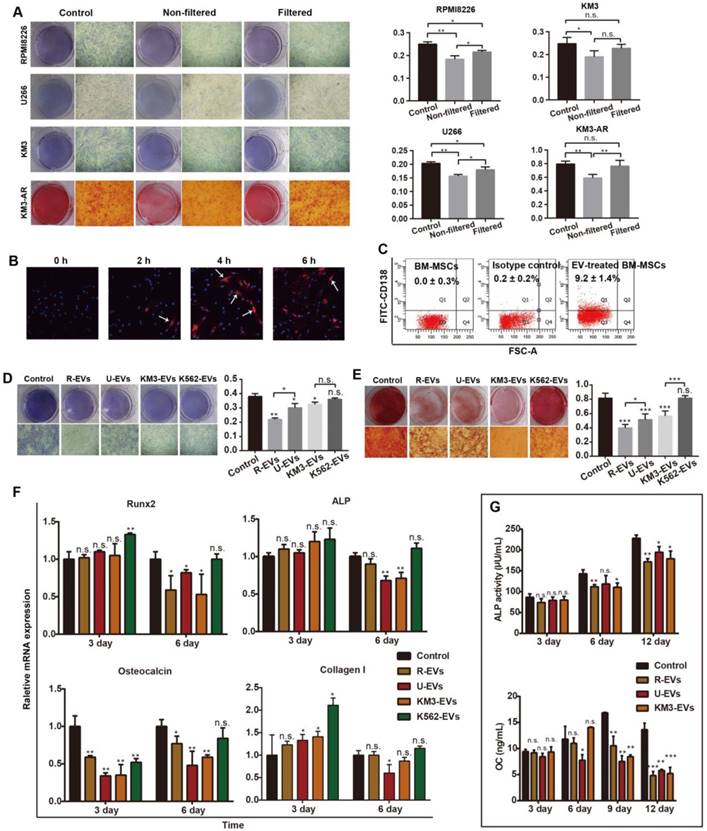
接着,研究人员试图确定MM-EV是否会影响BM-MSC的成骨功能。他们用80%成骨分化培养基和20%未过滤MM细胞培养基(RpMI 8226、U266和KM3)或条件细胞培养基(通过离心和过滤去除EV)处理BM-MSC。21天后,通过染色检查BM-MSC的成骨细胞克隆数CFU-OB,他们观察到未过滤的培养基比条件培养基具有更明显的抑制作用。这些结果表明,EV对BM-MSC发挥成骨抑制作用。其中,原代BM-MSC及成骨分化培养基购自赛业生物。
立即索取赛业生物小鼠胚胎干细胞和胚胎干细胞完全培养基的详细资料
他们随后用来自RpMI 8226(R-EV)、U266(U-EV)或KM3(K-EV)细胞的MM-EV直接处理BM-MSC。他们发现,BM-MSC经过MM-EV处理后的成纤维细胞和成骨细胞克隆数明显少于对照,其中,R-EV发挥最大的抑制作用。接着,他们检测了成骨相关生物标志物的改变。他们发现,四种基因(RUNX2、ALp、osteocalcin和collagen I)的表达水平被一种或所有的MM-EV明显拉低。这些结果确认了MM-EV抑制BM-MSC的成骨功能(图1)。
图1. MM-EV抑制BM-MSC的成骨功能
既然miRNA在调节成骨中发挥了重要作用,那么MM-EV是否诱导BM-MSC的miRNA表达变化?研究人员之后通过miRNA测序分析了这一点。他们发现,BM-MSC经过MM-EV处理后,变化最大的miRNA包括miR-181a-3p、miR-21-3p、miR-103a-3p和miR-107,其中miR-103a-3p对于成骨至关重要。通过实时定量pCR证实,R-EV诱导BM-MSC中miR-103a-3p的高表达。这表明此种miRNA可能与成骨抑制作用有关。
MM-EV让小鼠模型的骨髓瘤骨病恶化
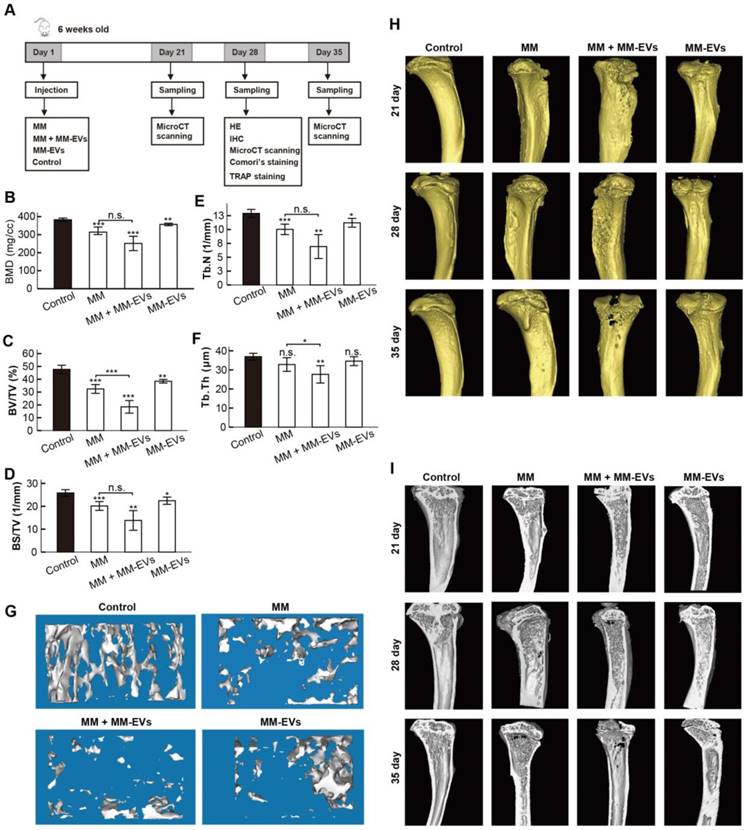
之后,研究人员开展了体内研究。他们将RpMI 8226细胞和/或R-EV直接注射到胫骨,建立了小鼠模型。Micro-CT显示,MM-EV组和MM组左胫骨骨干的骨密度等各项指标都明显低于对照组。染色结果也表明了严重的骨破坏和MM细胞浸润,以及MM组和MM+MM-EV组的成骨细胞更多,破骨细胞更少。这些结果说明,单次注射R-EV可以降低小鼠胫骨的成骨功能,与体外研究结果一致(图2)。
此外,R-EV还可以增强MM细胞的活性,加剧MM细胞诱导的成骨功能降低,并显著增加MM诱导的破骨细胞分化。这些结果支持了R-EV推动小鼠模型的疾病进展。
点击了解赛业生物小鼠模型
图2. 小鼠胫骨的Micro-CT分析
外周血CD138+ cirEV水平指示骨病变
最后,研究人员从新发骨髓瘤患者的外周血中分离出cirEV,以评估cirEV水平与BMD及其他骨髓瘤临床特征之间的关联。他们发现,CD138+ cirEV计数能够区分新发患者和健康供体。对于骨髓瘤骨病,他们还发现CD138+ cirEV计数与骨病变的数量有关,存在0处、≤ 3处和> 3处骨病变的患者在结果上明显不同。这些结果表明,外周血CD138+ cirEV计数是骨髓瘤骨病的潜在诊断标志物。
“虽然以往的研究认为细胞外囊泡在骨髓瘤中发挥了不同作用,但我们提出首个证据,表明MM-EV在体外抑制BM-MSC的成骨功能,并让小鼠的骨髓瘤骨病恶化,而外周血CD138+ cirEV对骨髓瘤骨病具有诊断意义,”作者在文中总结道。
原文检索:
Zhang L, Lei Q, Wang H, Xu C, Liu T, Kong F, Yang C, Yan G, Sun L, Zhao A, Chen W, Hu Y, Xie H, Cao Y, Fu F, Yuan G, Chen Z, Guo AY, Li Q. Tumor-derived extracellular vesicles inhibit osteogenesis and exacerbate myeloma bone disease. Theranostics 2019; 9(1):196-209. doi:10.7150/thno.27550.