Nature子刊:骨关节炎的发展与这种蛋白相关
骨关节炎(Osteoarthritis,简称OA)是中老年人中常见的一种退行性关节疾病。根据美国疾控中心的统计,在美国65岁以上的人群中,大约80%患有关节炎。软骨退化影响了骨关节炎的治疗。
近日,中国人民解放军总医院王岩教授和军事医学科学院北京生物工程研究所叶棋浓教授等人领导的研究团队对骨关节炎背后的分子机制进行了深入剖析。他们发现,HpIp(全名为造血前B细胞白血病转录因子相互作用蛋白)在骨关节炎的发展中起到重要作用。
这项成果于1月中旬发表在《Nature Communications》杂志上。“我们发现,HpIp通过Wnt信号通路的转录激活以及转录程序的表观遗传调控来调控软骨退化,表明HpIp有望带来骨关节炎治疗的新办法,”作者在文中写道。
之前的研究表明,HpIp蛋白主要在癌症发生和发展中起到调节作用。例如,乳腺癌中HpIp-ER组成的复合物网络在体内和内外促进了细胞增殖和迁移。此外,HpIp的沉默抑制了TGF-β诱导的上皮间充质转化。TGF-β是一种内源性的细胞因子,在维持软骨稳态上发挥调节作用。然而,HpIp在骨关节炎中的作用仍然未知。
HpIp敲除可防止骨关节炎发展
为了确定HpIp在骨关节炎中的作用,研究人员首先分析了118对骨关节炎软骨组织及相应非病变样本中HpIp的表达水平。通过免疫组化染色和qRT-pCR分析,他们发现骨关节炎软骨中HpIp的表达明显高于非病变组织。而且,HpIp的表达随着骨关节炎的发展而逐渐增加,而细胞外基质(ECM)组分COL2A1和ACAN的表达逐渐减少,表明它可能参与关节软骨退化中的ECM降解。
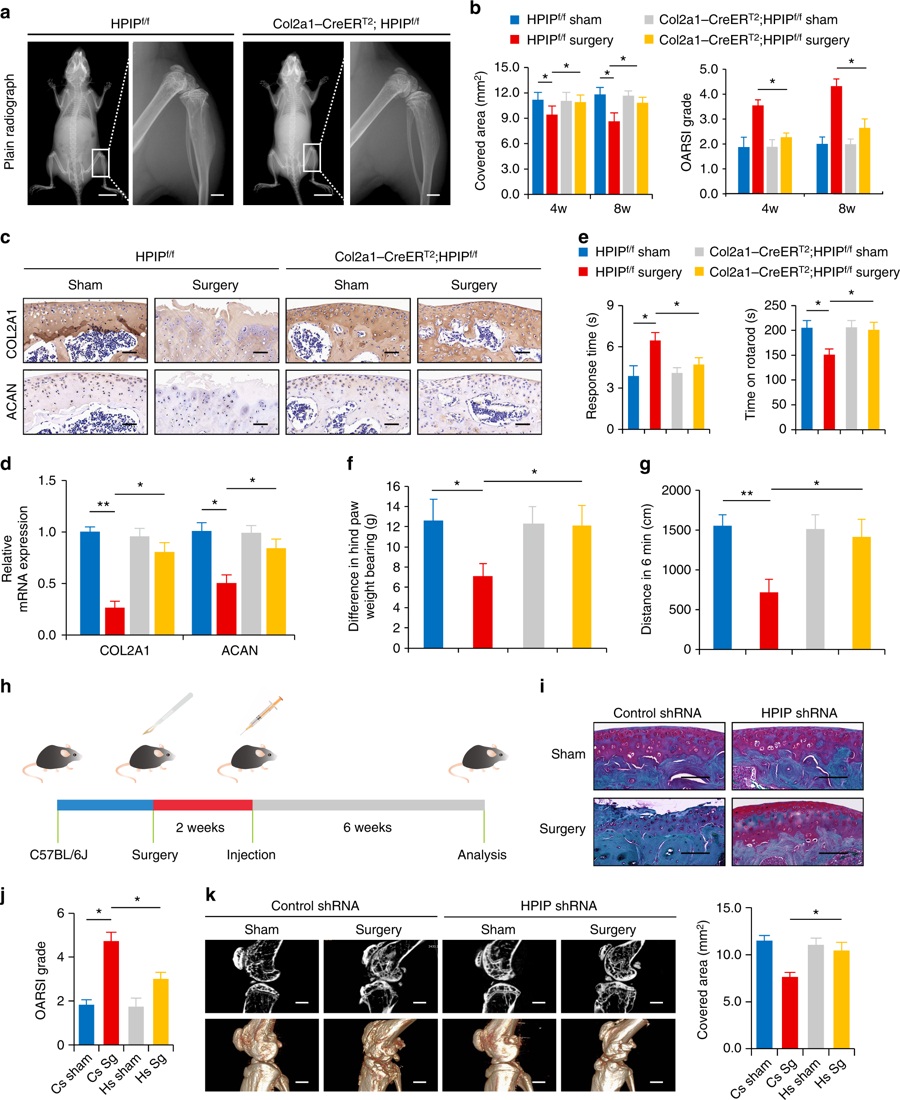
接下来,研究人员又分析了软骨细胞特异性HpIp敲除小鼠的表型。他们委托赛业生物(Cyagen)制备了HpIpf/f小鼠,又购买了Col2a1-CreERT2小鼠,从而制备出Col2a1-CreERT2/HpIpf/f小鼠。多个染色结果表明,与同窝的HpIpf/f小鼠相比,Col2a1-CreERT2/HpIpf/f小鼠表现出明显的骨骼异常。它们的肱骨、股骨、胫骨和椎骨等骨骼的长度比对照小鼠短10-21%。
那么,HpIp究竟在骨关节炎发病机制中扮演了什么角色?他们对Col2a1-CreERT2/ HpIpf/f小鼠和HpIpf/f小鼠实施手术,将其膝关节中的前十字韧带切除,并检查手术后的软骨厚度和覆盖面积。在手术后4周和8周时,HpIpf/f小鼠的软骨厚度和覆盖面积都低于Col2a1-CreERT2/HpIpf/f小鼠。
此外,骨关节炎的发展还伴有继发性的临床症状。转棒仪和热板分析和疼痛测定表明,HpIpf/f小鼠的热板响应时间增加,转棒仪响应时间、负重且行进距离减少,而经历或未经历手术的Col2a1-CreERT2/HpIpf/f小鼠在转棒仪或热板响应时间上没有差异。因此,这些结果表明HpIp的敲除可以防止骨关节炎的发展。
为了进一步研究HpIp在骨关节炎治疗中的作用,研究人员对8周龄的C57BL/6J野生型小鼠进行前十字韧带切除术。两周后,他们在关节内注射了AAV载体,此载体编码HpIp特异性的shRNA。结果表明,未接受注射的小鼠表现出更严重的软骨退化,并且软骨厚度和覆盖面积更低。这些结果表明HpIp特异性的shRNA可保护关节免受软骨损伤。
HpIp调控了哪些信号通路?
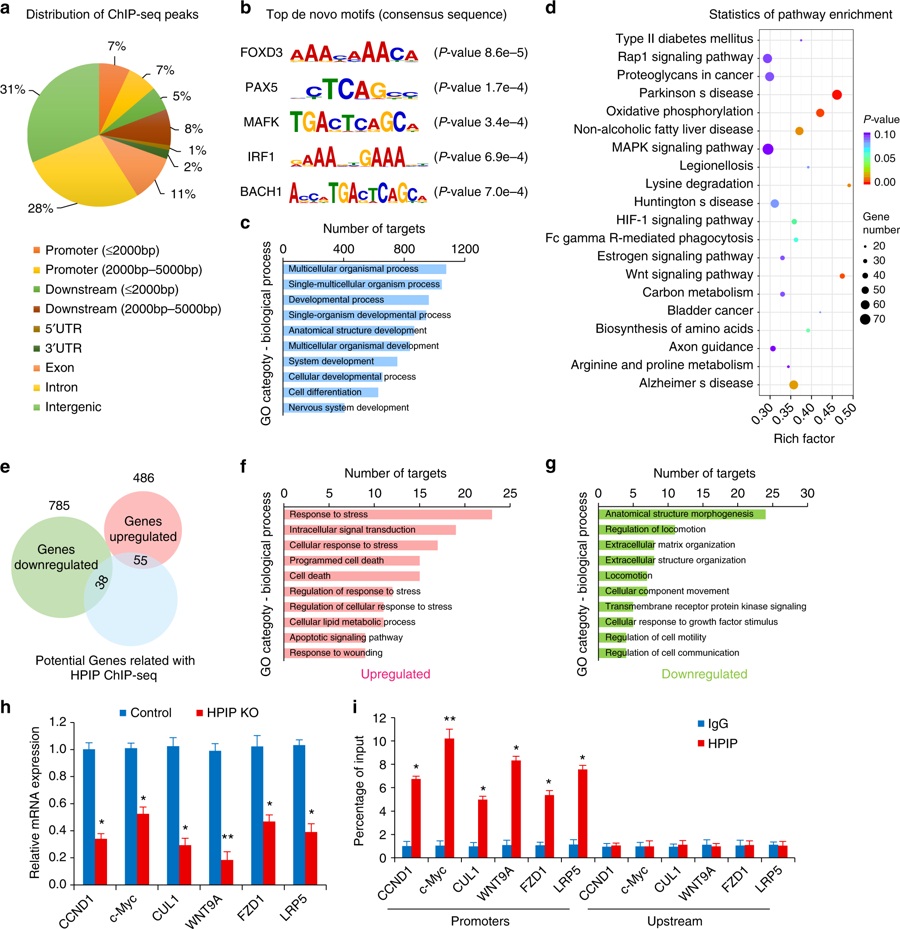
研究人员接着对HpIp敲除的软骨细胞和对照软骨细胞开展RNA-seq分析,以便确定HpIp调控的靶点。与对照细胞相比,HpIp敲除细胞存在1271个显著差异表达基因(DEG),其中486个基因的转录本上调,而包括COL2A1在内的785个基因转录本下调。此外,KEGG通路分析表明DNA复制、ECM-受体相互作用和Wnt信号通路下调,而p53信号通路上调。这些数据表明HpIp是维持软骨稳态的关键调节蛋白。
之后,他们又利用全基因组染色质免疫沉淀测序(ChIp-seq)来确定HpIp的直接靶点。结果显示HpIp存在3136个明显的ChIp-seq峰,包括pBX1。他们接着分析了ChIp-seq和RNA-seq数据的交集,发现有93个靶点受到HpIp缺失的直接调控。最终发现,在HpIp缺陷型的软骨细胞中,Wnt信号通路下游靶点的mRNA表达水平明显下调。
酵母双杂交和免疫共沉淀分析表明,HpIp与转录因子LEF1之间存在相互作用。HpIp过表达增加了Wnt多个靶点的表达,而内源性LEF1的敲低抑制了Wnt靶点的表达并消除了HpIp调控Wnt靶点的能力,表明LEF1对于HpIp介导的Wnt靶点调控是十分重要的。
由于组蛋白乙酰化通常与基因的活跃转录有关,故研究人员深入探讨了HpIp是否通过染色质状态的修饰来调控Wnt靶点表达。LEF1敲低降低了HpIp的招募以及多个基因的启动子上H3K56ac的乙酰化,表明H3K56ac活性对于HpIp调控基因转录是重要的。这些数据表明,HpIp能够直接激活Wnt信号通路上关键靶点的表达,具体方式是对其启动子上的H3K56ac进行乙酰化。
作者认为,这些结果表明HpIp有望成为骨关节炎的治疗靶点。不过,在未来开展临床试验之前,还需要进一步研究来评估编码HpIp特异性shRNA的慢病毒载体在大型骨关节炎动物模型上的功效。(生物通 余亮)
原文检索
Hematopoietic pBX-interacting protein mediates cartilage degeneration during the pathogenesis of osteoarthritis
Nature Communications 10, Article number: 313 (2019)