新突破!这种胶原蛋白可以遏制肿瘤转移
原发肿瘤切除后,如果术后辅助治疗不能完全清除残留的肿瘤细胞,这些肿瘤细胞就会通过血液循环到达远处的器官,定植并进入休眠状态。
几年后,休眠的肿瘤细胞会在特定条件下被激活。迅速增殖并形成明显转移。
一旦肿瘤细胞进入休眠状态,细胞周期停滞在G0/G1期,细胞不增殖,也不凋亡。
传统的放疗和化疗将失去效果,使肿瘤更难完全治愈。
因此,有学者提出它可以被激活,休眠的肿瘤细胞将被消灭。
问题是,休眠肿瘤细胞和原发肿瘤细胞的基因表达是不同的。原来的治疗计划可能对激活的细胞不起作用。匆忙激活休眠的肿瘤细胞可能会导致更糟的情况
因此,另一组科学家决定做相反的事情。要么让这批处于休眠状态的肿瘤细胞永久休眠,不让它们醒来,要么更无情地在它们处于休眠状态时直接消灭它们,这可能会防止肿瘤复发。
要使肿瘤细胞休眠,就必须了解其休眠的机制。
美国西奈山伊坎医学院的一个研究小组最近在《自然癌症》杂志上发表了一项研究,揭示了细胞外基质在肿瘤微环境中对肿瘤细胞进入和保持休眠状态的关键作用。

研究人员首先从休眠的肿瘤细胞巢开始,探索这种肿瘤微环境的特殊之处是什么,使肿瘤细胞在这里睡觉?
采用尾静脉注射的方法将休眠肿瘤细胞系和增殖肿瘤细胞系接种到小鼠体内。
与小鼠体内迅速形成肿瘤的增殖肿瘤细胞不同,休眠肿瘤细胞在小鼠体内通常以单细胞形式出现。以细胞或惰性结节的形式出现。
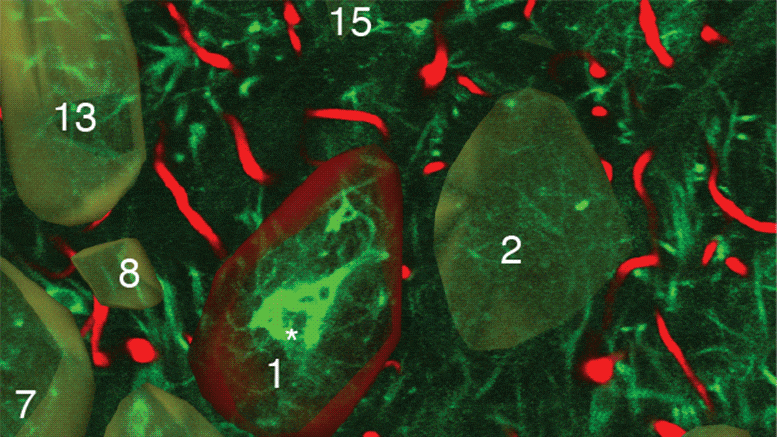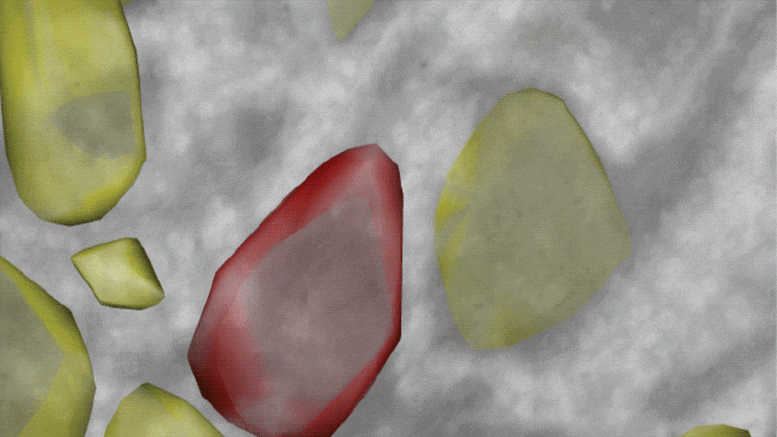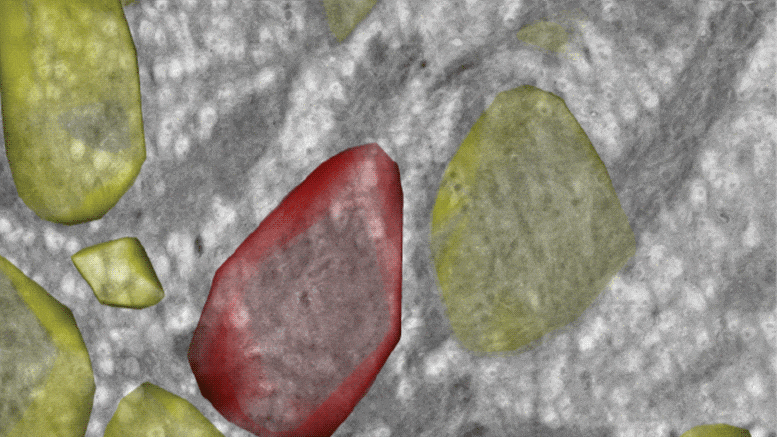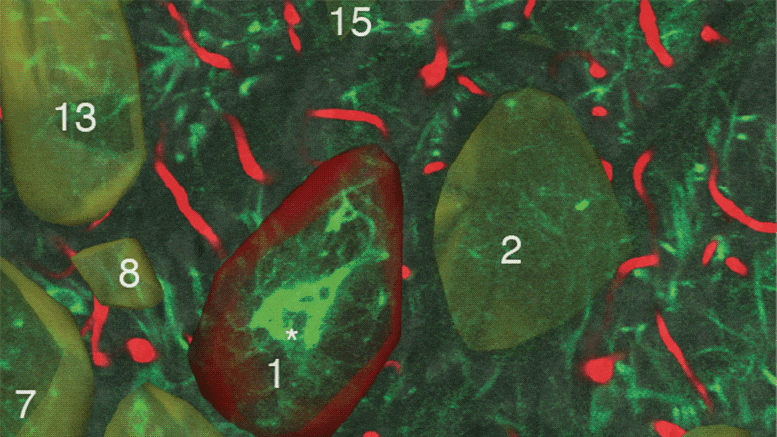
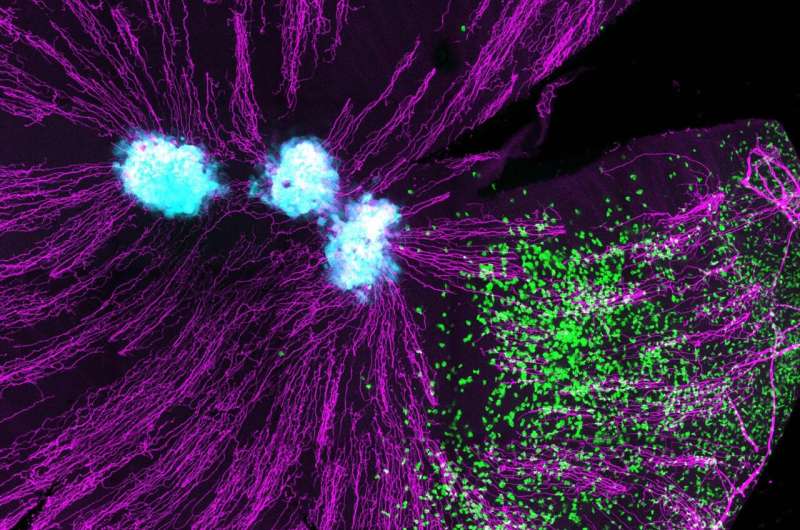
在多光子二次谐波成像下,研究人员观察到:
休眠的肿瘤细胞外基质主要由卷曲无序的胶原纤维组成,而增殖的肿瘤细胞外基质胶原纤维呈直线排列,更具方向性。
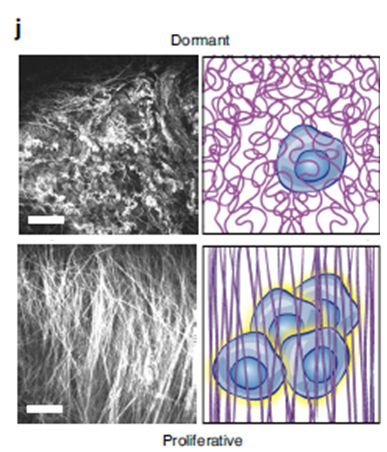
随着肿瘤的发展,肿瘤细胞外基质中胶原纤维的排列也发生了动态变化。
肿瘤发展得越深入,卷曲的胶原纤维就变得越整齐。
更令人惊讶的是,当研究人员将增殖的肿瘤细胞接种到小鼠体内时,肿瘤被手术切除,以模拟接受肿瘤手术的患者的临床治疗。
在手术伤口边缘有少量残留的肿瘤细胞。当这些残留的肿瘤细胞原位复发或远处转移,并从休眠状态进入增殖状态时,细胞周围的胶原纤维也发生了由卷曲到直的变化。
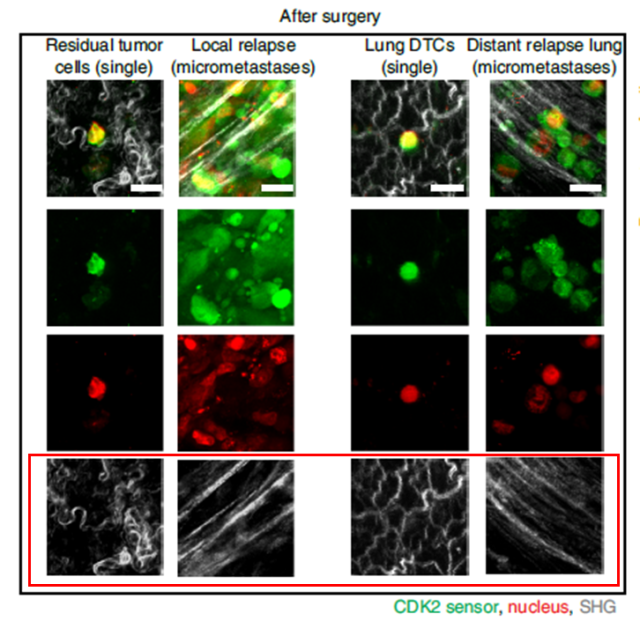
左:肿瘤原位复发;右:肿瘤肺转移复发
这些结果表明细胞外基质的结构与肿瘤细胞的休眠-恢复状态密切相关。
休眠肿瘤细胞周围的胶原蛋白呈卷曲分布,休眠细胞恢复增殖后,周围的胶原蛋白呈线性分布。
进一步,研究人员对脱细胞的肿瘤团块进行质谱分析,研究处于休眠和增殖状态的肿瘤细胞的细胞外基质组成的差异,发现与增殖的肿瘤细胞相比,在休眠肿瘤细胞外基质中发现III型胶原。
肿瘤细胞含量明显增加,对肿瘤细胞的转录组分析也显示COL3A1在休眠肿瘤细胞中的表达增加。
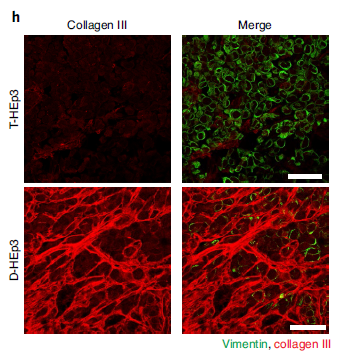
III型胶原(红色荧光)、T-HEp3增殖头颈部鳞状细胞癌细胞系、D-HEp3休眠头颈部鳞状细胞癌细胞系
同时,对临床头颈部鳞癌患者的原发肿瘤部位活检显示,有淋巴结转移的患者原发肿瘤部位的III型胶原蛋白水平高于无转移的患者。低。
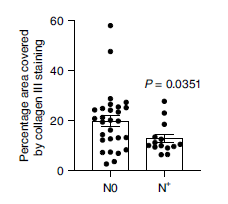
图例:N0例肿瘤患者无淋巴转移,N例肿瘤患者有淋巴转移
以上结果表明,肿瘤微环境中III型胶原含量越高,肿瘤细胞越容易休眠,而III型胶原含量越低,肿瘤细胞越活跃,越容易转移。
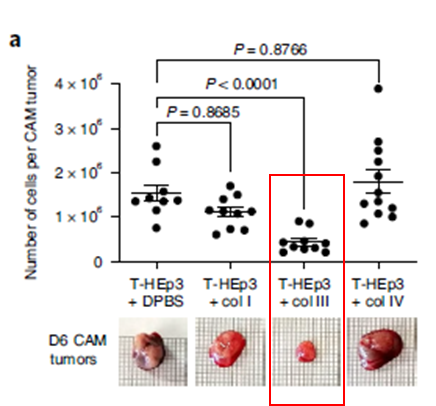
下一步,为了证明III型胶原是否是肿瘤细胞进入休眠状态的关键,研究人员将增殖的肿瘤细胞与I型胶原、III型胶原、IV型胶原结合,将杜尔贝科磷酸盐缓冲溶液(DpBS)接种到鸡绒毛尿囊膜中,发现:
与III型胶原联合注射的肿瘤细胞形成较小的肿瘤肿块,与肿瘤细胞增殖相关的组蛋白H3磷酸化下调,核蛋白p27(一种休眠标记物)表达增加,表明III型胶原抑制肿瘤细胞增殖并诱导肿瘤细胞进入休眠状态。
接下来,为了验证III型胶原是否能抑制原发肿瘤切除部位残留肿瘤细胞的增殖,研究人员用浸润III型胶原的牙科海绵覆盖肿瘤切除部位,对照组用浸润海绵的DpBS覆盖相应部位,追踪了两组小鼠局部肿瘤的复发情况,发现:
植入III型胶原生物支架的小鼠只有20%肿瘤复发,而对照组小鼠肿瘤复发的概率为80% !
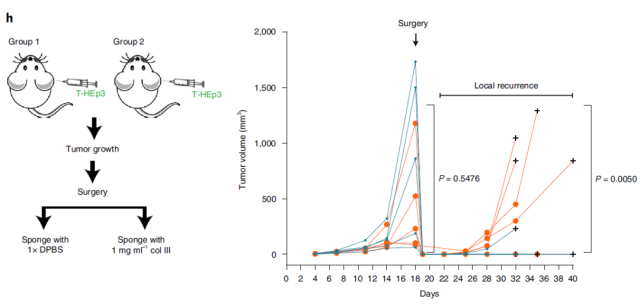
蓝色:III型胶原蛋白组,橙色:DpBS组术后肿瘤局部复发
更重要的是,III型胶原蛋白不仅能抑制肿瘤增殖,诱导肿瘤细胞进入休眠状态,而且是维持肿瘤细胞休眠状态的关键。
敲除休眠肿瘤细胞的COL3A1基因后,休眠肿瘤细胞不再休眠,植入后迅速增殖生长。
然而,如果增生性肿瘤细胞过表达COL3A1,则细胞增殖受到抑制,植入后形成的肿瘤体积较小。再次证明了III型胶原蛋白在肿瘤细胞休眠期间是必不可少的。
最后,为了找出III型胶原利用哪些信号通路诱导和维持肿瘤细胞休眠,研究者通过一系列基因敲除和抢救实验发现,III型胶原与休眠的肿瘤细胞存在一定的关系。积极的反馈路径:
休眠III型胶原与肿瘤细胞的DDR1受体结合,激活STAT1进入细胞核,促进COL3A1的表达,肿瘤细胞分泌III型胶原,肿瘤细胞保持休眠状态。

总之,这项研究揭示了肿瘤微环境对肿瘤细胞休眠的影响,表明III型胶原在这项研究中,扮演着重要的角色和III型胶原蛋白的肿瘤微环境促进肿瘤细胞进入和维护处于休眠状态。,抑制肿瘤增殖。
使肿瘤患者体内残留的肿瘤细胞处于休眠状态,可以避免肿瘤复发,延长患者的生存期。
未来,III型胶原蛋白可能在临床上作为预测肿瘤复发的标志物和维持肿瘤细胞休眠、防止肿瘤复发的治疗方法。
( III型胶原蛋白在肿瘤微环境中只能起到促进休眠的作用。没人认为口服III型胶原蛋白就可以抗癌,对吧?)