季红斌组合作揭示小细胞肺癌细胞亚型转变导致转移机制
1月5日,国际学术期刊National Science Review在线发表了中国科学院分子细胞科学卓越创新中心季红斌研究组和中国科学院数学与系统科学研究院王勇研究组合作的最新研究成果“Identification of TAZ as the essential molecular switch in orchestrating SCLC phenotypic transition and metastasis”。在该项工作中,研究人员揭示调控小细胞肺癌细胞亚群转变及转移的关键分子TAZ及其作用机制。
小细胞肺癌是恶性程度最高的肺癌亚型,极易发生远处转移。小细胞肺癌患者5年存活率约7%,与其高转移密切相关。目前对于负责小细胞肺癌转移的细胞亚型及其调控机制不甚清楚。利用自发小鼠模型,研究人员发现小细胞肺癌原发瘤内存在异质性:部分肿瘤细胞呈现神经粘附分子NCAM高表达、基质细胞分子CD44低表达,即NCAMhiCD44lo/-表型特征;而另一些肿瘤细胞则呈现NCAM低表达CD44高表达,即NCAMloCD44hi表型特征。此外,远端转移灶一致呈现出NCAMhiCD44lo/-表型特征,暗示该细胞亚群可能负责小细胞肺癌转移。后续肿瘤转移小鼠实验验证了这一猜想。有意思的是,NCAMloCD44hi细胞随着肿瘤恶性进展会转变为NCAMhiCD44lo/-细胞从而获得高转移潜能。
机制研究发现,随着小细胞肺癌恶性进展Hippo 信号通路核心分子TAZ受染色质重塑复合物SWI/SNF调控并发生下调,引发NCAMloCD44hi亚群向NCAMhiCD44lo/-亚群发生转变,并最终促进小细胞肺癌转移。TAZ激活可以反向地促进NCAMhiCD44lo/-亚群向NCAMloCD44hi亚群发生转变,从而抑制小细胞肺癌转移。
这些动物模型中的发现进一步得到临床数据的支持。公共单细胞测序数据分析表明,小细胞肺癌转移灶中大多数肿瘤细胞呈现NCAMhiCD44lo/-特征。中国人临床样本分析进一步发现,NCAMhi/CD44lo/-/TAZlo表达特征与更差的患者预后紧密相关。
综上所述,该研究发现NCAMhiCD44lo/-亚群负责小细胞肺癌转移,其来源于TAZ下调引发的细胞亚群转变,而TAZ在细胞亚群转变及小细胞肺癌转移中发挥重要的分子开关作用。该研究为深入理解小细胞肺癌转移机制奠定了坚实的理论基础。
中国科学院分子细胞科学卓越创新中心金宇娟副研究员、赵琪琪博士、冯艳博士,中国科学院数学与系统生物学研究院朱炜康和深圳大学肖田副教授为该论文的共同第一作者;中国科学院分子细胞科学卓越创新中心季红斌研究员、胡良副研究员和中国科学院数学与系统科学研究院王勇研究员为该论文共同通讯作者。该工作得到分子细胞科学卓越创新中心刘新垣研究员、陈洛南研究员、朱学良研究员、张雷研究员、高栋研究员,肺科医院张鹏教授,上海交通大学姜丽岩教授,中国科学院营养健康研究院秦骏研究员,复旦大学附侯英勇教授、李飞教授,纽约大学Kwok-Kin Wong教授和Hua Zhang博士,科隆大学Roman K Thomas教授等支持。该研究还获得了国家自然科学基金、国家重点研发计划和中科院战略性先导科技项目等资助。
文章链接:https://academic.oup.com/nsr/advance-article/doi/10.1093/nsr/nwab232/6496053?searchresult=1#
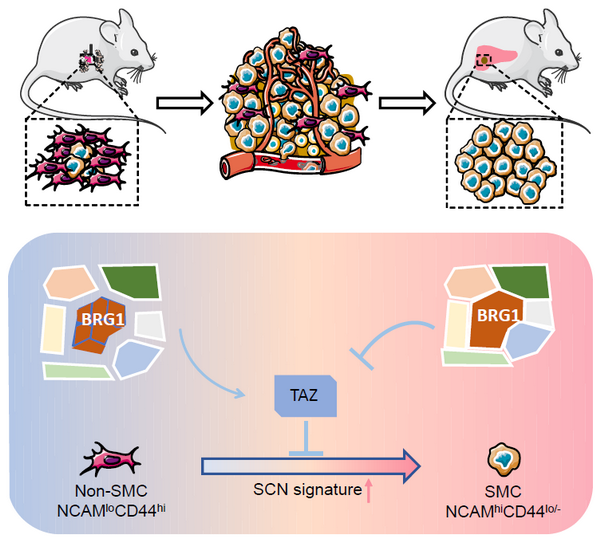
TAZ调控小细胞肺癌亚群转变及转移的模式图






























