基础医学院白丽教授课题组揭示了Foxo1在iNKT细胞不同功能亚群的发育分化和功能调控中的作用差异
iNKT (invariant natural killer T)细胞是重要的免疫调控细胞,在肿瘤、代谢性炎症、感染等多种疾病中发挥重要调控作用。根据产生细胞因子和关键转录调控因子的不同,iNKT细胞主要分为iNKT1、iNKT2和iNKT17三个亚群。但是,三种iNKT细胞亚群的发育和功能是否受不同机制调控仍不清楚。
2021年11月16日,中国科学技术大学白丽教授课题组在proceedings of the National Academy of Sciences (pNAS)发表题为“iNKT subsets differ in their developmental and functional requirements on Foxo1”的研究论文,揭示了Foxo1在iNKT细胞不同功能亚群的发育分化和功能调控中的作用差异。
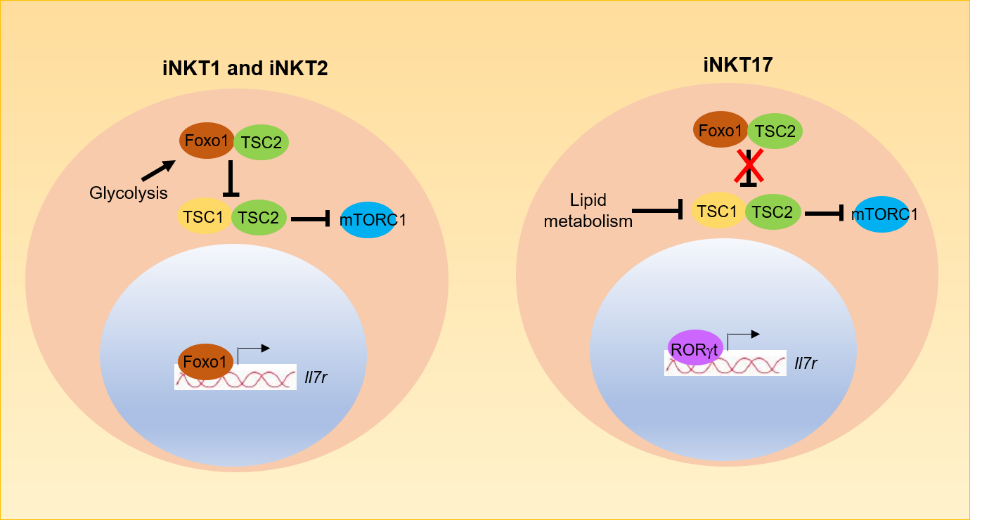
Il7-IL7R信号对iNKT细胞的发育、存活起到关键调控作用。该项研究发现转录因子Foxo1 (forkhead box protein O1)通过调控IL7R表达促进iNKT1和iNKT2亚群的早期发育分化,而iNKT17亚群的发育分化不依赖Foxo1。iNKT17细胞IL7R表达受转录因子ROR?t调控,而非Foxo1。对iNKT1、iNKT2和iNKT17三个亚群的发育分化路径分析发现,三个亚群的命运决定发生在iNKT细胞发育分化的早期即祖细胞阶段(iNKT progenitors)。在此阶段,Foxo1对iNKT细胞亚群分化发挥了不同作用。缺失Foxo1的不成熟的iNKT1和iNKT2细胞明显减少,Bcl2和Il7r的表达明显降低,而iNKT17亚群的发育及Bcl2和Il7r的表达不受影响。此外,iNKT1和iNKT2的活化也受到Foxo1调控。在iNKT1和iNKT2亚群中,细胞质中Foxo1通过与TSC2结合抑制TSC1-TSC2相互作用,从而促进mTORC1的活化。但是,iNKT17亚群中TSC1-TSC2的相互作用以及mTORC1的活化不受Foxo1调控。同时该工作还发现,iNKT1和iNKT2亚群的糖酵解促进Foxo1从细胞核定位到细胞质进而抑制TSC1-TSC2相互作用,促进mTORC1活化,而脂肪酸代谢对iNKT17亚群TSC1-TSC2的相互作用起到重要调控作用。
中国科学技术大学特任副研究员张会敏为该文章第一作者,白丽教授为通讯作者。该项研究工作获得了国家自然科学基金委,科技部,中国科学技术大学的大力支持。
文章链接:https://www.pnas.org/content/118/46/e2105950118






























