刘文贤教授课题组在Science Advances发文揭示调控胸腺成熟T细胞...
不管是目前火热的以CAR-T、pD1抗体疗法为代表的新型肿瘤免疫治疗策略,还是在新冠病毒感染后T细胞直接清除病毒或辅助B细胞分泌中和抗体,均揭示了T细胞亚群是清除肿瘤和对抗病毒感染的关键细胞亚群,这也意味着T细胞在数量和功能上的正常对于维持机体正常的免疫状态至关重要。T细胞自胸腺发育而来,在胸腺中经历beta选择、阳性选择、阴性选择等一系列“检查点”筛选后,仅有2%-5%的胸腺T细胞发育成熟而从胸腺迁出到外周免疫器官。值得一提的是,胸腺T细胞在阴性选择后期到进入成熟状态准备迁出之前,经历了TCR信号(CD69)下降,同时迁移信号(S1p1)上升的生理进程,这一精密的生理进程调控了胸腺成熟T细胞迁出至外周。然而何种信号机制调控该进程还所知甚少。
2021年10月8日,细胞应激生物学国家重点实验室刘文贤教授、付国教授课题组,在Science Advances杂志上发表了题为“Glycogen synthase kinase 3 drives thymocyte egress by suppressing β-catenin activation of Akt”的研究论文,揭示了GSK3/β-catenin信号通路在调控胸腺成熟T细胞从胸腺迁出的重要功能和调控机制,为T细胞发育和迁移的信号调控提供新的分子机制解析。

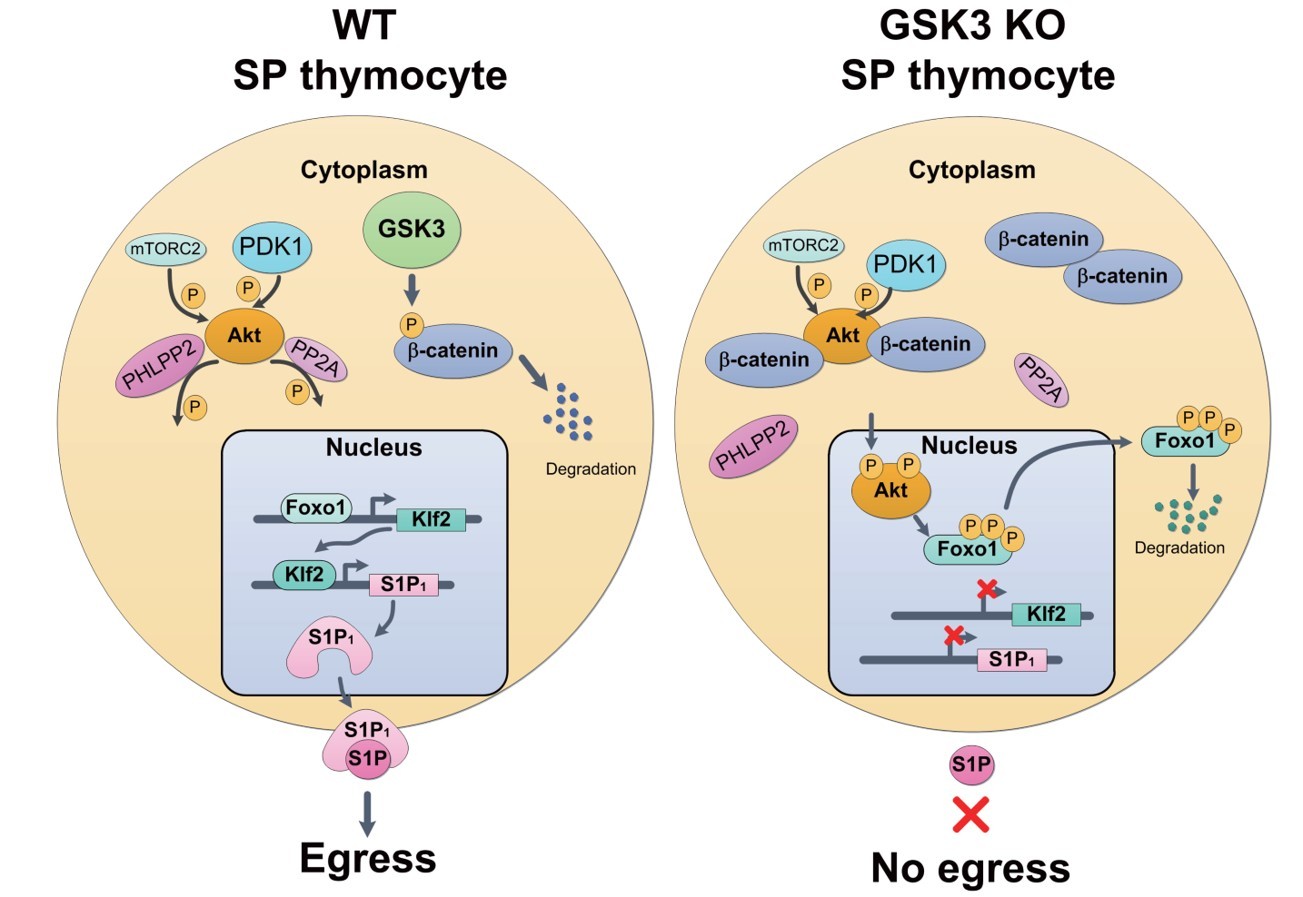
Wnt/β-catenin信号通路已知在维持干细胞特性、细胞分化等具有重要作用,该信号异常激活能够促进细胞恶性增殖等形成肿瘤。糖原合成酶激酶3(GSK3)包含两个亚基:GSK3α和GSK3β,其可以与ApC、AXIN1、CK形成复合体,能够磷酸化β-catenin导致其泛素化降解,以此维持了Wnt/β-catenin信号通路在机体内的正常表达和行使功能。自1981年GSK3被发现以来,已经证明了其在神经系统、骨骼新生、糖尿病、肿瘤中发挥多种生物学功能。但是其在T细胞生物学中的研究还有待深入。研究人员利用GSK3afl/fl,GSK3bfl/fl;CD4Cre(DKO)小鼠分析发现,DKO小鼠外周免疫器官中T细胞几近消失,利用胸腺细胞示踪技术发现,DKO小鼠胸腺成熟T细胞迁移出现明显缺陷。通过转录组学结合蛋白水平分析发现,DKO小鼠胸腺T细胞中Foxo1/KLF2/S1p1信号通路出现明显缺陷,该通路是已知的调控胸腺成熟T细胞迁出的重要通路,进一步分析发现,GSK3缺失后导致Akt激酶异常激活,是介导Foxo1/KLF2/S1p1通路缺陷的主要原因。为了证明该条信号通路的正确性,研究人员利用骨髓改造降低Akt激酶活性,或者引入持续激活的转录因子Foxo1AAA,均能够有效的回补GSK3缺失导致的迁移缺陷。研究人员接下来探究GSK3如何调控Akt激酶活性,结果发现,胞浆内高表达的β-catenin可以直接促进Akt激酶激活,机制上研究人员发现,胞浆内的β-catenin主要减低Akt和其去磷酸酶pHLpp2和pp2A的互作,从而抑制pHLpp2和pp2A对Akt的去磷酸化,以此促进了Akt激酶活性。综上,该研究首次报道了GSK3在调控胸腺成熟T细胞迁出的重要作用,并且在免疫细胞中首次揭示了β-catenin不依赖经典的转录调控而直接在胞浆内激活Akt的新型调控机制。以上工作不仅丰富和完善了胸腺成熟T细胞迁出的调控机制,同时胞浆β-catenin直接促进Akt活性的机制,也为包括白血病、淋巴瘤在内的多种肿瘤在恶性增殖、复发耐药等机制的探索中提供新的理论参考。
院刘文贤教授、肖昌春教授和付国教授是本文的共同通讯作者,博士生刘晨风、马蕾和王雨萱是本文的共同第一作者。本项研究得到了厦门大学实验动物中心和生物医学学部仪器平台的重要支持,受到国家自然科学基金,厦门大学校长基金等资助。
论文全文链接:https://www.science.org/doi/10.1126/sciadv.abg6262






























