周德敏团队在长效靶向调节性T细胞的细胞因子类药物治疗自身免疫性疾病研究方面取得重要进展
2021年9月27日,北京大学药学院周德敏教授团队与协和医院免疫风湿科张烜教授团队合作,在学术期刊Nature Biomedical Engineering上,发表了题目为“Site-specific pEGylation of interleukin-2 enhances immunosuppression via the sustained activation of regulatory T cells”的研究论文,介绍在长效靶向调节性T细胞的细胞因子类药物治疗自身免疫性疾病方面取得的重要进展。
自身免疫病是一类人体自身免疫系统攻击正常细胞并造成免疫能力异常,最终导致器官功能性障碍的慢性炎症性疾病。目前,广谱的免疫抑制剂、激素等仍为临床上普遍应用的治疗方案,其副作用强、药效个体化差异等问题困扰着自身免疫病的治疗,研发新型的自身免疫病治疗性药物具有重要意义。
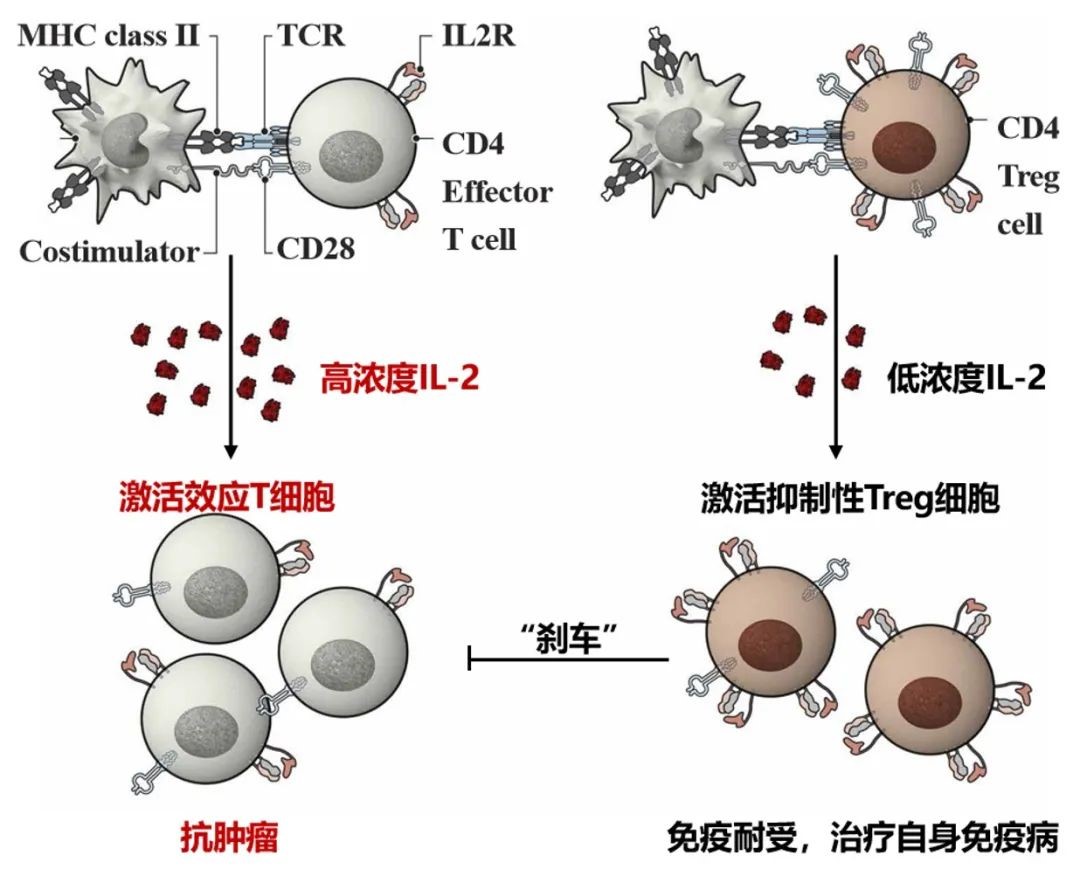
IL-2的通过激活效应细胞及调节T细胞,兼具免疫抑制及免疫激活双重作用
白细胞介素-2(Interleukin-2)是一种可作用于多种淋巴细胞的关键细胞因子。低剂量注射白细胞介素-2(IL-2)通过偏向性激活调节T细胞(Treg),可以起到有效的抑制病理性免疫和治疗自身免疫病的效果;然而由于IL-2的多效性,不适剂量的IL-2也会非靶向地激活效应细胞和免疫系统,加速疾病进程。同时,IL-2分子量小半衰期短,需要频繁注射给药以维持自身免疫病治疗所需要的低剂量有效浓度。数十年来IL-2因其复杂的药物性质及可能导致的严重副作用,严重限制了这种有潜力的细胞因子在自身免疫病治疗中的应用。如何有效解决IL-2的上述问题,提高其在自身免疫病等炎症类疾病中的有效性和安全性构成了亟待解决的关键科学问题。
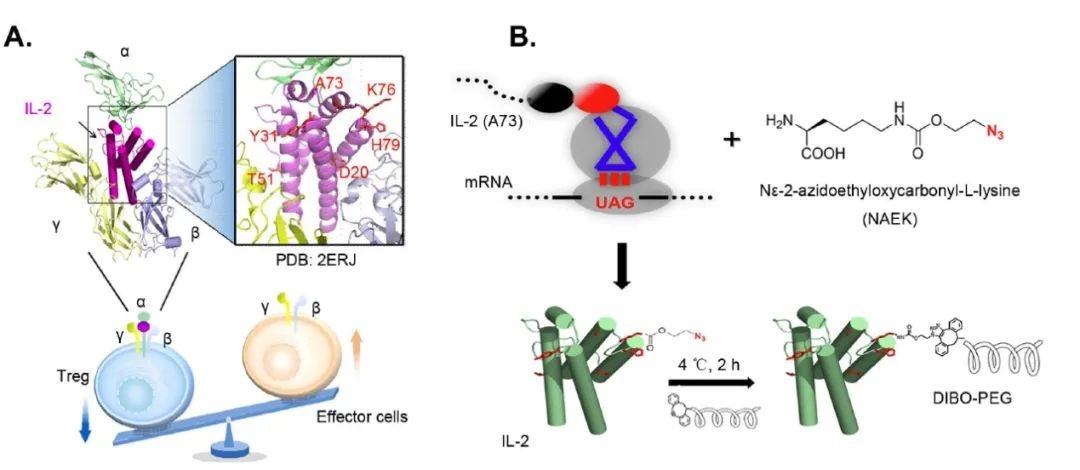
精准修饰IL-2类药物对调节性T细胞的靶向激活作用示意图
周德敏团队与协和医院免疫风湿科张烜团队合作,利用基因密码子扩展技术对IL-2蛋白进行精准的聚乙二醇(pEG)修饰,调整IL-2与其三种亚型受体的亲和力和偏向性,实现持久且靶向性地激活调节性T细胞(Treg)、减轻炎症反应的目标。基础实验结果表明,在IL-2的Y31和T51位点同时进行20K-pEG修饰,其对IL-2Rβ的亲和力明显降低,表现出对Treg细胞的靶向激活作用。临床前实验表明精准pEG修饰不仅实现了药物的均一性和提高了血清稳定性,还拓展了药物的治疗窗,在类风湿性关节炎、系统性红斑狼疮、移植物抗宿主病等多种疾病模型中表现出良好的治疗效果,扩宽了细胞因子IL-2类大分子药物在免疫治疗中的应用前景。

周德敏团队博士生张博(2016年毕业,现协和医院工作)、孙家琦(直博生)、王妍(2020年毕业,现朝阳医院工作)、纪德重(在站博士后)等为论文的共同第一作者,周德敏教授和张烜教授为共同通讯作者。这项研究得到科技部、国家自然基金委和重大新药创制科技重大专项多个基金的长期支持。
【延伸阅读】
论文链接:https://www.nature.com/articles/s41551-021-00797-8

周德敏 教授,博士生导师 任北京大学药学院院长、天然药物及仿生药物国家重点实验室主任。教育部长江学者,国家科技部领军人才及中组部万人计划创新团队负责人,973首席科学家、基金委创新群体负责人、国家重大新药创制专项负责人。长期从事基于化学-生物学交叉的新药发现新技术、新方法研究,聚焦病毒和细胞动态修饰介导的免疫治疗和基因治疗、内源性大分子定点修饰的成药性研究等方向。全国首届优秀博士论文获得者,曾担任美国化学会Mol pharm杂志副主编、J Med Chem杂志国际编委,《中国药学(英文版)》的执行主编。在Science、Science Adv、pNAS等杂志发表论文百余篇,十多项国内外专利和企业合作进入应用开发阶段;疫苗研究成果获评“中国科学十大进展”。
(北京大学药学院 天然药物及仿生药物国家重点实验室)






























