Nature:是什么告诉细胞血脂水平低了,从而引发一系列活动防止饥饿?

彼得·道格拉斯博士(右)和研究生阿比盖尔·沃特森
德克萨斯大学西南分校的研究人员发现了一种分子途径,这种途径可以让细胞在脂质供应耗尽时感知到,从而引发一系列活动来防止饥饿。发表在《自然》杂志上的这一发现,可能有一天会导致对抗代谢紊乱和各种其他健康状况的新方法。
德克萨斯大学西南分校分子生物学助理教授、研究负责人彼得·道格拉斯博士说:“脂质是提供能量的关键,是细胞膜和其他细胞结构的组成部分。”“我们发现的机制似乎是一种让细胞普遍测量脂质水平的方法,而无需区分各种不同的脂质类型。”
道格拉斯博士是德克萨斯大学西南分校哈蒙再生科学和医学中心的成员,他解释说,哺乳动物的细胞拥有成千上万种不同类型的化学性质不同的脂类,这类分子由碳氢链组成,是体内能量最丰富的化学物质。20世纪90年代,德克萨斯大学西南诺贝尔奖得主迈克尔·布朗(Michael Brown)和约瑟夫·戈德斯坦(Joseph Goldstein),两位分子遗传学和内科学教授,发现了第一个脂质感应通路:SREBp通路,它通过感应一种叫做固醇的脂质来帮助细胞调节胆固醇水平。
SREBp途径中的成分通过直接结合固醇分子实现这一功能。然而,为了适应不同类型的脂质,道格拉斯博士说,细胞中可能存在额外的感知机制。
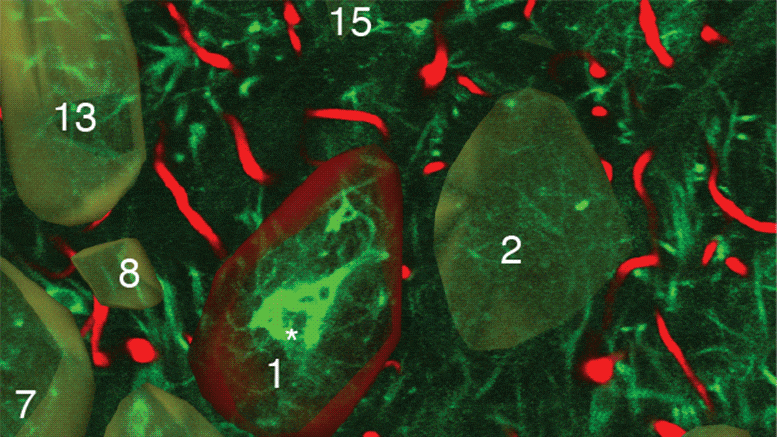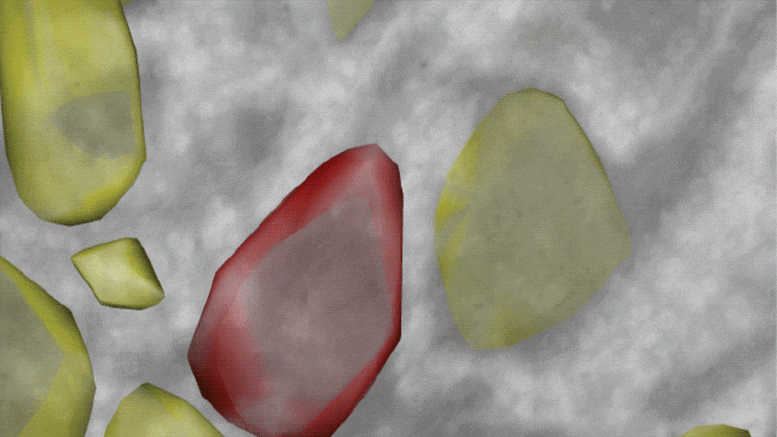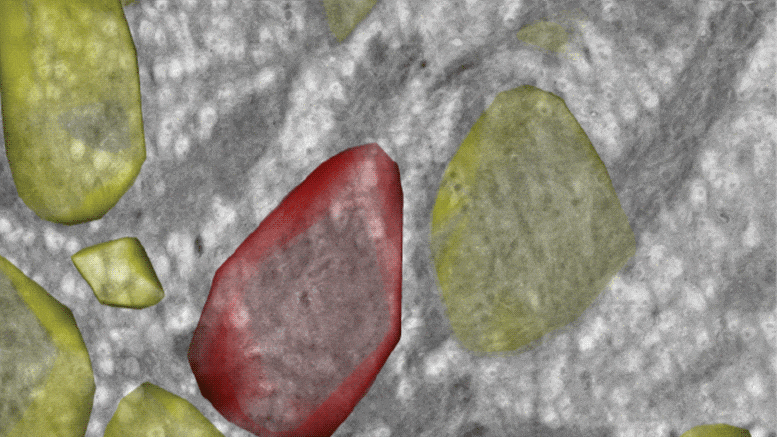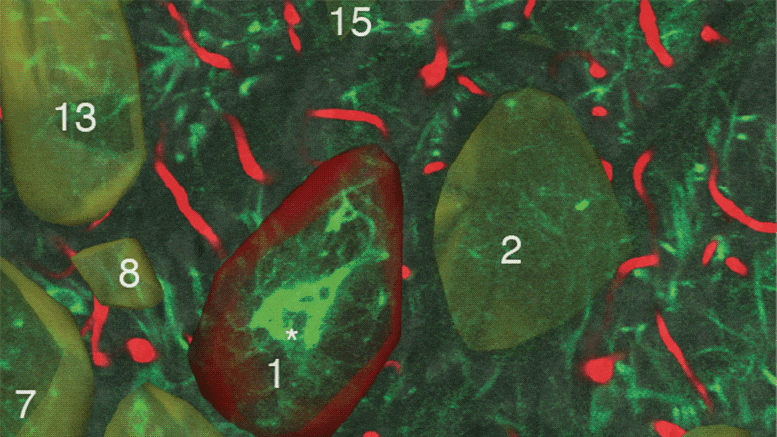
为了寻找一种细胞可能普遍适用于感知脂质水平的机制,研究人员让秀丽隐杆线虫(Caenorhabditis elegans)挨饿。秀丽隐杆线虫是一种蛔虫,是一种常见的实验室模型,与人类共享许多基因。当这些动物被剥夺食物24小时,研究人员发现一种被称为核激素受体49 (NHR-49)的蛋白质从细胞溶质(细胞液体部分)到了细胞核,这引发了一连串的基因活性,促使其他蛋白质运输细胞表面收集细胞外营养物质。
研究人员发现,当秀丽隐杆线虫吃饱时,NHR-49 被一种称为 RAB-11.1 的蛋白质固定在原位。这种蛋白质属于被称为小 G 蛋白的一类,由已故的 Alfred G. Gilman 博士发现,他是诺贝尔奖获得者和 UTSW 的长期药理学主席,后来担任医学院院长、执行官负责学术事务的副校长兼教务长。但在饥饿条件下,RAB-11.1 释放了 NHR-49,允许其进入核。
进一步的实验表明,这种释放是由缺乏一种称为香叶基香叶基焦磷酸的脂质触发的。 Douglas 博士解释说,由于细胞可以使用几乎任何脂质作为起始材料来制造香叶基香叶基焦磷酸盐,因此它的存在可作为细胞中可接受的脂质水平的通用信号。
他补充说,其他实验室先前的研究表明,该途径的成分在许多疾病和健康问题中都很活跃,包括代谢疾病、心血管疾病、病毒感染、神经老化和一些癌症。道格拉斯博士说,操纵这种新的脂质传感途径最终可能会导致针对这些疾病的新疗法。
原文标题:
Intracellular lipid surveillance by small G protein geranylgeranylation