【快报第92期】基础医学研究所黄粤和余佳团队发现胚胎干细胞退出多能性的转录后调控新机制
2020年12月22日[HY1],中国医学科学院基础医学研究所黄粤和余佳团队在The EMBO Journal发表了“hnRNpLL controls pluripotency exit of embryonic stem cells by modulating alternative splicing of Tbx3 and Bptf”的论文。研究报道了hnRNpLL通过调控Bptf、Tbx3等关键基因mRNA的可变剪接促进胚胎干细胞退出多能性的转录后调控新机制。
胚胎干细胞(Embryonic stem cell, ESC)具有可体外培养、无限增殖、自我更新和多向分化的特性,在适当条件下可诱导生成不同类型的细胞、组织。ESC从多能性状态退出、打破维持ESC多能性的调控网络,是ESC进入谱系分化程序的首要步骤。转录后调控(post-transcriptional gene regulation,pTGR)是真核基因表达调控的重要环节。有研究指出,pTGR启动了ESC多能性的退出,因为自我更新相关基因mRNA水平的迅速下降,早于其转录水平的沉默。而RNA的各种转录后调控过程均由RNA结合蛋白(RNA binding protein,RBp)参与和介导完成。
该研究工作系统性筛查了RBp在ESC退出多能性中可能的功能,发现7个RBp的缺失会不同程度影响小鼠ESC退出多能性。其中,hnRNpLL缺失会导致ESC在分化状态下自我更新基因不能正常下降,ESC的体内、外分化能力严重受损,过表达hnRNpLL则能显著促进ESC退出多能性。
hnRNpLL互作蛋白质组分析发现其在ESC中主要与RNA剪接复合体相互作用,可能参与调控RNA剪接。进一步对hnRNpLL-/- ESC中RNA可变剪接及hnRNpLL所结合靶RNA进行系统分析,发现hnRNpLL促进了一系列在ESC退出多能性过程中增加的可变外显子跳跃(exon skipping)事件,而hnRNpLL的缺失则抑制了这些可变外显子的跳跃,导致退出多能性障碍。随后作者详细研究了hnRNpLL对重要多能性调控因子Tbx3和Bptf mRNA可变剪接的调控。发现Tbx3 exon2a 和Bptf exon24a均是可变外显子,包含该可变外显子的转录本起到维持ESC多能性的作用,而不包含该外显子的转录本则发挥相反功能,hnRNpLL则通过抑制该可变外显子的选择促进ESC退出多能性。在hnRNpLL-/- ESC中特异敲除Tbx3 exon2a 和Bptf exon24a则能部分恢复其退出多能性的缺陷。通过本研究,作者认为hnRNpLL所介导的RNA可变剪接在ESC多能性退出中发挥关键作用,为研究转录后调控在ESC多能性退出中的功能机制提供了有价值的资源和参考,并提出了可通过靶向RBp优化ESC体外分化系统、加速ESC再生医学应用的新途径和思路。
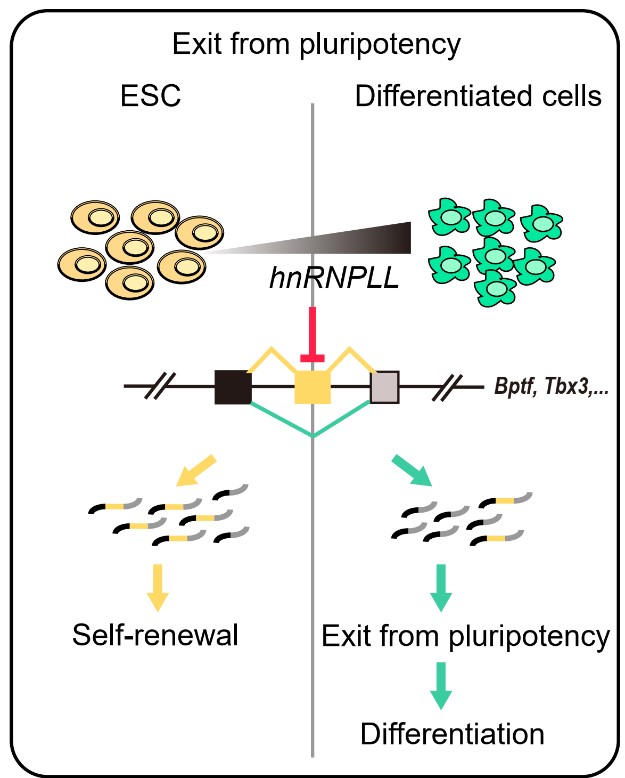
图1. hnRNpLL通过调控Bptf、Tbx3等关键基因mRNA的可变剪接促进ESC退出多能性
本研究工作得到中国医学科学院医学与健康科技创新工程(2016-I2M-3-002, 2019-I2M-2-001,2017-I2M-3-009)等项目的资助。中国医学科学院基础医学研究所黄粤研究员、余佳研究员、马艳妮副研究员和南方医科大学王栋研究员为论文共同通讯作者,中国医学科学院基础医学研究所王雪博士后、平昌昀博士研究生和南方医科大学谭普文博士研究生为论文的共同第一作者。
论文链接:https://www.embopress.org/doi/epdf/10.15252/embj.2020104729






























