顾宏周团队开发利用环化酶高效制备DNA单环和拓扑结构的新技术
环状单链脱氧核糖核酸(circular ssDNA)在分子生物和DNA纳米技术等领域扮演着重要的角色,如作为滚环扩增的必备模板、DNA拓扑结构的构成单元等。目前常用的依赖于T4 DNA连接酶制备环状单链DNA的方法容易产生多聚体副产物,导致单体环产率低;而现有的基于CircLigase(一种单链环化酶)制备环状单链DNA的方法虽然可一定程度上减少副产物,但是随着底物DNA链长度的增大,CircLigase催化成环的效率急剧下降。因此,高效率地制备单链环形DNA仍是一个亟待解决的问题。
2020年12月31日,我院顾宏周团队在Analytical Chemistry杂志发表了题为“programming CircLigase Catalysis for DNA Rings and Topologies”的论文,报道了一种基于CircLigase高效制备DNA单环和拓扑结构的新技术。这一技术主要通过在单链DNA末端设计杂交的结构使得CircLigase参与的酶促反应由不可控的熵变主导转为可控的焓变主导,从而高效率(>75%产率)无副产物地合成DNA单环。该技术不仅将CircLigase的催化DNA成环产率稳定地提升至75%以上,而且突破了CircLigase对于可环化的DNA片段的长度的限制,在几百碱基的长链DNA上都得到了验证。课题组同时利用CircLigase预制备的单链DNA环作为起始组装材料获得了高纯度的DNA拓扑嵌套结构。

文章中首先确定了末端杂交结构对高效成环的必要性,测试了一系列参数:如反应温度、末端互补配对碱基数、末端不配对碱基个数和末端碱基种类等对成环效率的影响,并建立了可以被CircLigase催化高效成环的单链DNA模型。文章中还进一步地研究确定了对于较长(例如200至500个碱基)单链DNA底物链,末端杂交结构同样能帮助其高效成环。
此外,该团队进一步研究发现末端杂交结构可以从DNA分子内转移至DNA分子间,即末端杂交结构也可提高两条不同单链DNA分子间的连接效率。并且末端杂交结构可以由单链DNA底物自身互补配对提供,也可以通过一条辅助DNA链与单链DNA底物末端配对形成,两种杂交方式连接效率相当。随后,又提出末端结构通过拉近单链DNA底物5’和 3’端距离,从而提高CircLigase催化成环效率的猜想。
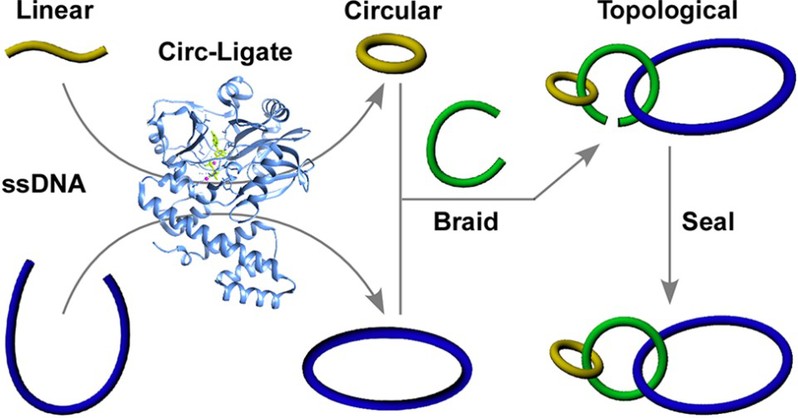
综上,该团队提出了一种简单有效的在单链DNA末端设计杂交结构的策略提升CircLigase催化DNA成环的效率,而高产率和高纯度制备环状DNA不仅在纳米技术方面有潜在应用,也可用来筛选更加稳定的作为肿瘤诊断和治疗的新一代核酸适配体。值得一提的是,CircLigase本身在病毒中作为一种RNA连接酶。由于DNA与RNA化学结构相似,因此该研究中设计末端杂交结构提高CircLigase环化DNA效率的策略理论上也适用于RNA底物。利用这套策略原则上也可以稳定高效地合成天然存在的环状RNA分子,以便在体外研究其结构和功能。
复旦大学生物医学研究院研究生李青婷为第一作者,顾宏周研究员为通讯作者。
原文链接:https://pubs.acs.org/doi/10.1021/acs.analchem.0c04668






























