生命学院José C. Pastor-Pareja课题组报道果蝇内质网-高尔基体结构组成
蛋白质分泌对于真核生物的形态发生和生理过程至关重要。在早期的分泌途径中,蛋白质货物先在内质网出口处被收集,经一系列高度保守的膜出芽及融合相关蛋白的共同作用转运至高尔基体。内质网-高尔基体转运过程受精密的调控,多年来的研究已经让我们从遗传和生化的角度较详尽地了解了内质网-高尔基体物质交换途径及背后的分子机制[1]。然而,胶原等巨型货物的早期分泌机制仍不清晰,内质网-高尔基体的结构组成以及介导货物运输的膜载体类型等问题仍有待解决。
2021年9月14日,清华大学生命学院José C. pastor-pareja课题组在《Cell Reports》杂志上发表了题为“果蝇内质网出口处有大量的囊泡和珠状小管,但没有巨型载体(ER exit sites in Drosophila display abundant ER-Golgi vesicles and pearled tubes but no megacarriers)”的研究论文,该文报道了果蝇脂肪体及翅膀盘的内质网-高尔基体结构组成,发现了参与双向运输的、与高尔基体相连的前顺式高尔基体区域,在内质网出口-高尔基体区域内发现大量的囊泡和珠状小管,并且没有发现巨型运输载体 (图1)。
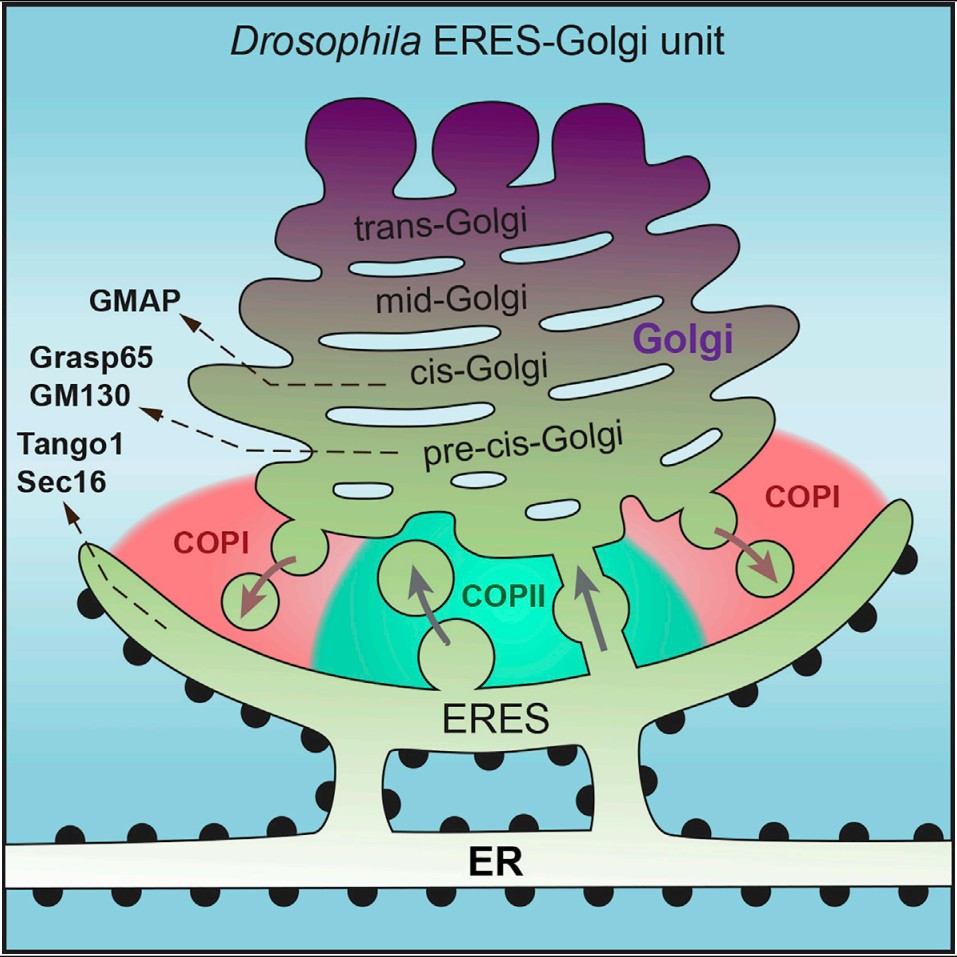
图1.果蝇内质网-高尔基体单元的结构组成
此研究主要使用转基因果蝇、三维结构照明显微镜、透射电子显微镜和聚焦离子束扫描电子显微镜(FIB-SEM)技术描绘果蝇内质网-高尔基体单元的结构组成,其中囊泡蛋白在内质网出口(ERES)-高尔基体界面呈现COpII中心/COpI四周型分布,与此前在毕赤酵母中的报道相似[2],随后的药物实验提示两者存在功能联系。在果蝇内质网-高尔基体单元内发现了区别于顺式高尔基体的前顺式高尔基体区域,前顺式高尔基体区域可被Grasp65和GM130标记,遗传学实验表明该区域为内质网-高尔基体间双向运输所需要。随后,通过对FIB-SEM观察的果蝇脂肪体和翅膀盘的内质网-高尔基体单元进行三维重构(图2),进一步描绘了果蝇内质网-高尔基体单元的基本结构特征,并发现在翅膀盘内过表达Tango1可以增加ERES区域的大小,这与Tango1在界定ERES中的作用一致[3]。

图2.果蝇脂肪体组织内质网-高尔基体单元的FIB-SEM观察及三维重构
此外,三维重构发现在分泌胶原的脂肪体以及翅膀盘中的内质网-高尔基体区域有大量囊泡和出芽结构,囊泡直径均呈现双峰分布(图3),这两群囊泡在内质网-高尔基体界面呈中心、四周型分布。同时,在内质网-高尔基间存在联通内质网与高尔基体的珠状小管结构(图3),与近期报道的哺乳细胞内内质网-高尔基体串珠样载体相似[4],并且没有发现巨型运输载体。本研究提示果蝇同时存在囊泡运输和管状运输,为从进化角度进一步理解蛋白质早期分泌途径以及胶原等巨型货物的运输机制提供了重要依据。
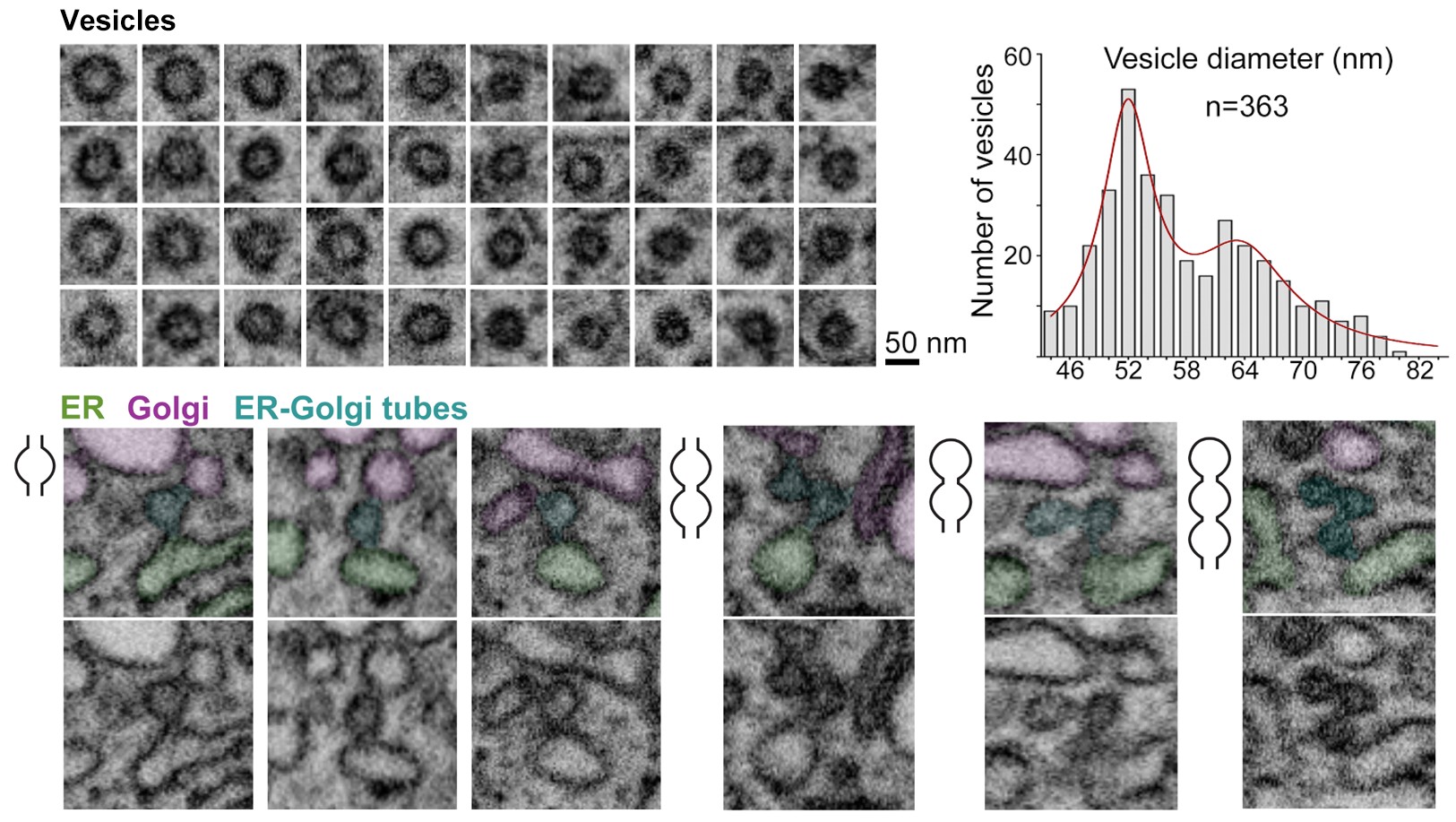
图3. 果蝇翅膀盘内的囊泡和珠状小管结构
此项研究工作使用转基因果蝇和高分辨成像技术详尽描绘了果蝇脂肪体和翅膀盘内质网-高尔基体单元的结构组成,文章的主要发现对理解蛋白质早期分泌途径有重要意义。
清华大学生命学院José C. pastor-pareja研究员为本文的通讯作者,清华大学生命学院2018级博士生杨珂和清华大学生命学院博士后刘敏为本文并列第一作者,课题组成员冯智、Marta Rojas、周玲建和柯红梅参与了研究工作。本项研究得到了清华大学设施蛋白质冷冻电镜平台的支持,受到清华-北大生命科学联合中心和国家自然科学基金委的资助。
原文链接:http://doi.org/10.1016/j.celrep.2021.109707
José Carlos pastor-pareja 实验室:http://joselab.life.tsinghua.edu.cn
延伸阅读:
1. Mironov, A.A., and Beznoussenko, G.V. (2019). Models of Intracellular Transport: pros and Cons. Front Cell Dev Biol 7, 146.
2. Roy Chowdhury, S., Bhattacharjee, C., Casler, J.C., Jain, B.K., Glick, B.S., and Bhattacharyya, D. (2020). ER arrival sites associate with ER exit sites to create bidirectional transport portals. J Cell Biol 219.
3. Liu, M., Feng, Z., Ke, H., Liu, Y., Sun, T., Dai, J., Cui, W., and pastor-pareja, J.C. (2017). Tango1 spatially organizes ER exit sites to control ER export. J Cell Biol 216, 1035-1049.
4. Weigel, A.V., Chang, C.L., Shtengel, G., Xu, C.S., Hoffman, D.p., Freeman, M., Iyer, N., Aaron, J., Khuon, S., Bogovic, J., et al. (2021). ER-to-Golgi protein delivery through an interwoven, tubular network extending from ER. Cell 184, 2412-2429 e2416.






























