2021年10月1日宋海与沈立课题组合作发现小细胞肺癌肿瘤内异质性及耐药性建立的新机制
小细胞肺癌(SmallCell Lung Cancer, SCLC)约占肺癌发病患者的15%,同时又属于神经内分泌癌的一种,其恶性程度高、生长速度快、转移早而广泛,五年存活率极低,是人类致死率最高的癌症之一。由于小细胞肺癌病人肿瘤转移早,因此通常不进行手术治疗,主要治疗方案以铂类药物与依托泊苷联合治疗为主,近40年来针对其治疗手段未取得突破性进展。小细胞肺癌起初对化疗十分敏感,但几乎不可避免地在一年内产生耐药性并复发。近年研究发现,小细胞肺癌具有高度的肿瘤内异质性,表现为除了具有大量神经内分泌样(neuroendocrine, NE)肿瘤细胞,还有少量非神经内分泌样(non-neuroendocrine, Non-NE)肿瘤细胞。但是小细胞肺癌异质性建立的调控机制、不同类型细胞间如何交互作用、异质性与耐药性的关系尚不清晰。
2021年10月1日,我院宋海课题组与沈立课题组合作在Science Advances上发表了题为YAp drives fate conversion and chemoresistance of small cell lung cancer的文章,对小细胞肺癌肿瘤内异质性和耐药性的产生的机制进行了深入的探索,为治疗小细胞肺癌提供了新的理论依据。
在多种肿瘤中,Hippo通路的共转录激活因子YAp/TAZ的表达上调或被激活,进而促进肿瘤的发生与发展。然而在小细胞肺癌中,90%以上的肿瘤样本或神经内分泌样肿瘤细胞系中均检测不到YAp/TAZ的表达,且YAp/TAZ表达水平与神经内分泌标记物的表达成负相关。为了揭示YAp在小细胞肺癌中的作用,研究人员利用单细胞测序和免疫组织化学等方法对肺神经内分泌细胞特异敲除p53、Rb及pten的小鼠小细胞肺癌动物模型进行分析,发现小细胞肺癌起始时所有的肿瘤细胞均呈现神经内分泌性质。然而,随着肿瘤的发展,Non-NE肿瘤细胞逐渐出现,比例随着肿瘤的进展而增加。进一步,研究人员构建了受四环素诱导YAp表达的小鼠小细胞肺癌动物模型,发现在小细胞肺癌细胞中激活YAp显著抑制小细胞肺癌的神经内分泌样基因表达,并促使NE肿瘤细胞转分化为Non-NE肿瘤细胞。在对该现象的机理研究中,研究人员发现小细胞肺癌中YAp的表达能显著的激活NOTCH信号通路。此外,还作者发现YAp不仅可以通过激活NOTCH信号通路抑制小细胞肺癌的神经内分泌性质,也可以直接激活REST/NRSF的表达进而抑制小细胞肺癌的神经内分泌性质,促使NE细胞转分化为Non-NE细胞。
同时,研究人员还发现YAp激活的肿瘤细胞对化疗药物Cisplatin和Etoposide产生了明显的耐药性。在耐药性的研究中,研究人员发现Non-NE肿瘤细胞较于NE肿瘤细胞对于化疗药物具有更强的耐药性。深入的探索发现,该差异是由化疗药物处理后两类细胞发生不同的死亡方式所造成的。Non-NE肿瘤细胞在化疗药物处理后发生经典的凋亡,而NE肿瘤细胞发生GSDME所介导的细胞焦亡。进一步的研究表明,小细胞肺癌中YAp的激活能明显抑制GSDME的表达,从而抑制焦亡发生进而使小细胞肺癌具有更强的耐药性。
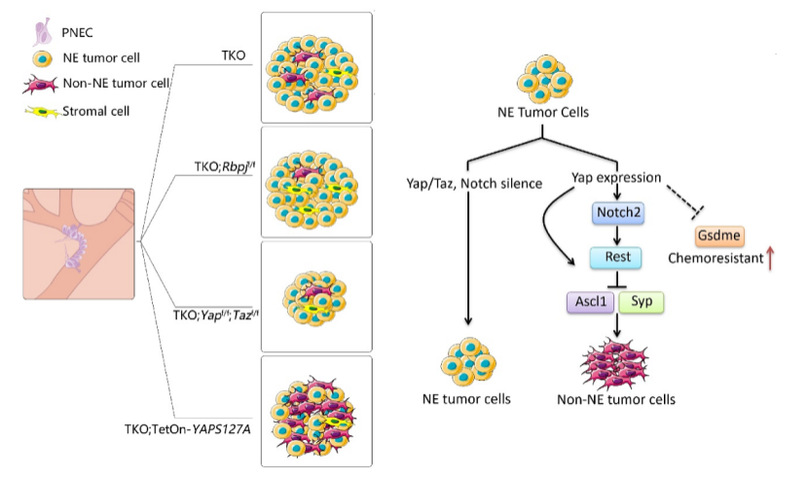
图1:YAp调控小细胞肺癌异质性与耐药性
综上所述,该研究揭示了YAp/TAZ的激活以及与NOTCH信号通路互作在小细胞肺癌肿瘤内异质性及耐药性建立的调控机制。尽管该研究揭示了YAp在小细胞肺癌中的一部分功能,但是还有很多问题亟待解决。例如,YAp在小细胞肺癌发展过程中是如何从无到有被表达出来的;化疗药物是如何诱导YAp的表达;NE与Non-NE肿瘤细胞之间如何相互转分化及互作的,这些问题的解决将加深对YAp在小细胞肺癌中作用的理解。
浙江大学生命科学研究院博士后吴庆哲、博士生郭晶鑫和刘聿宁为文章的共同第一作者,宋海教授和沈立教授为共同通讯作者。
原文链接:https://www.science.org/doi/10.1126/sciadv.abg1850






























