使用小分子蛋白复合物标记干细胞,实现高时空分辨率活体示踪
干细胞疗法在临床试验中被用于皮肤损伤、血液和心血管疾病、软骨缺损、糖尿病等多种疾病的治疗。然而,由于干细胞治疗的复杂性,其疗效及安全性一直存在质疑。其中,干细胞在体内的药代动力学未知,是被质疑的主要问题之一。
目前,干细胞追踪常用的pET-CT、MRI成像有价格昂贵、时间空间分辨率有限、通量低等劣势。近年来,活体近红外二区(NIR-II,1000-1700 nm,活体穿透深度~1cm)荧光成像为细胞示踪提供了新思路。然而,目前使用的NIR-II细胞示踪剂多为无机纳米材料,具有代谢困难及长期滞留所产生的潜在毒性等问题。
近日,中国科学院上海药物研究所分子影像中心程震、陈浩团队与南方科技大学李凯副教授课题组合作,设计出基于NIR-II小分子染料蛋白复合物的干细胞示踪剂(CelTrac1000),用于标记并示踪干细胞在不同疾病环境中的响应和命运。CelTrac1000使用可代谢的NIR-II小分子染料(CH-4T)与穿膜肽(Tat)修饰的人血清白蛋白 (HSA)1:1复合而成,形态类似于上市药物紫杉醇白蛋白(Abraxane等),具有制备生产精确可控、量子产率高、毒性低和可代谢等优点。相关成果于2021年6月19日发表于Research期刊。

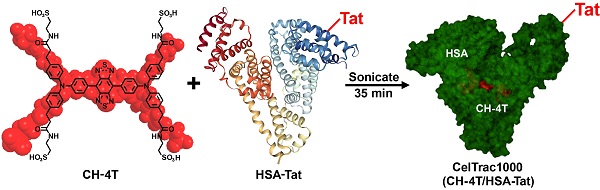
图1、 CelTrac1000的制备过程及结构示意图
合作团队利用该探针对人诱导多潜能干细胞-衍生内皮细胞(ipSC-ECs)1个月内体内血管生成进行可视化,评估了ipSC-ECs移植再生的治疗效果。为验证该方法的时间空间分辨率,研究人员利用CelTrac1000标记小鼠间充质干细胞(MSC)进行了体内动态示踪,并清晰地看到被标记的MSC在血液循环系统中的实时迁移过程。该方法实现了无创小鼠体内单细胞团簇运动、右肺四小叶肺叶呼吸扩张、以及心脏搏动的可视化监测。
最后,研究人员利用CelTrac1000实现了三种疾病模型——急性肺损伤 (ALI)、心肌梗死 (MI) 和大脑中动脉闭塞 (MCAO)中MSC的示踪(图2)。由于MSC具有趋向受伤部位组织富集的特点,利用CelTrac1000标记细胞,可观察尾静脉注射的MSC在疾病小鼠体内的生物分布。有趣的是,该研究发现肺损伤同时会引起小鼠心脏的损伤,而心脏损伤时不会引起肺损伤。此外,研究同时发现了MSC对脑部炎症的响应。
综上,本项研究表明CelTrac1000可用于标记干细胞,同时实现NIR-II高时空分辨率活体示踪,为揭示干细胞在体内的药代动力学机制提供了助力。
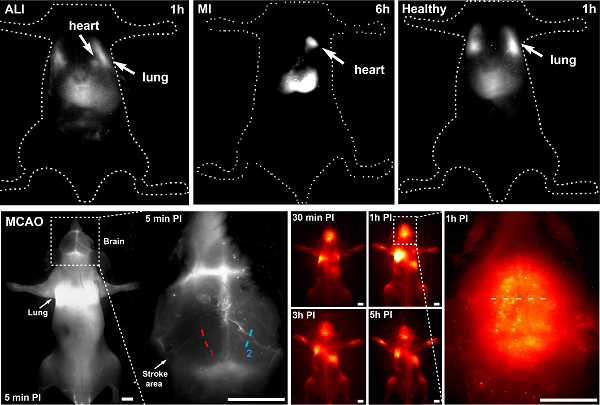
图2、急性肺损伤 (ALI)、心肌梗死 (MI) 和大脑中动脉闭塞 (MCAO)中MSC的示踪
上海药物所分子影像中心陈浩研究员为本研究的第一作者,南方科技大学李凯副教授、上海药物所分子影像中心程震研究员为通讯作者。该研究获得了国家自然科学基金,上海市浦江人才,上海市科技重大专项等项目的资助。
全文链接:https://spj.sciencemag.org/journals/research/2021/9798580/
(供稿部门:陈浩课题组;供稿人:汪志明)






























