新型lncRNA能够抵消心力衰竭
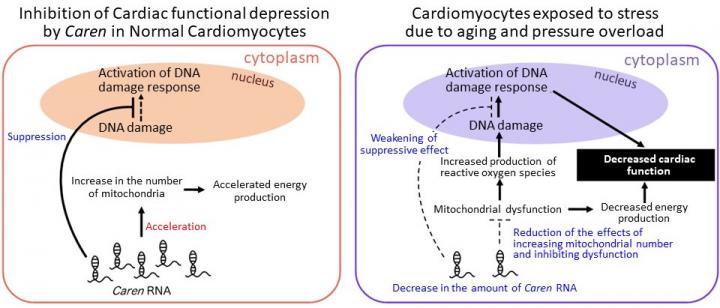
一个基于熊本大学(日本)的研究合作已经鉴定出一种新的在心肌细胞中大量表达的LncRNA,Caren。他们发现,它通过增加心肌细胞线粒体的数量来增强能量的产生,并抑制ATM蛋白的激活,ATM蛋白是DNA损伤反应途径中的一个关键角色,加速了心力衰竭的严重程度。心肌细胞中的Caren-RNA因衰老和高血压(高血压)而减少,高血压可导致心力衰竭,心力衰竭患者的心脏中的Caren-RNA明显减少。研究人员认为,心肌细胞中Caren的激活可能导致新的心力衰竭治疗方法的发展。
心力衰竭是指心肌泵血功能(收缩和扩张)降低,无法向身体泵入足够的血液。它仍然是一种预后不良的疾病,全世界心力衰竭患者的数量正在增加。在发达国家,心力衰竭患者数量的增加,尤其是老年人,是一个主要问题。因此,有必要制定有效的新治疗策略。
线粒体产生的能量对维持心脏功能至关重要。衰老和高血压增加了心力衰竭的发生几率,导致心肌细胞线粒体功能障碍,导致线粒体能量生成减少和活性氧生成增加。活性氧引起DNA损伤,随后激活DNA损伤反应,导致心力衰竭的加重。因此,线粒体功能障碍和DNA损伤反应的激活都是引起心力衰竭的重要原因。
熊本大学教授Oike领导的一个研究小组在小鼠心肌细胞中发现了一种新的LncRNA,并命名为Caren(心肌细胞富集的非编码转录本)。他们还发现,小鼠心肌细胞中的Caren-RNA数量因应激而减少,从而导致心力衰竭。进一步分析Caren在小鼠心脏中的作用,发现Caren能抑制心脏泵功能的下降。因此,研究人员认为,衰老和应激会减少心肌细胞中Caren-RNA的数量,从而降低其作用,促进线粒体功能障碍和DNA损伤反应的激活,从而导致心力衰竭的发展和恶化。
然后,研究人员通过基因工程设计出一种非致病性腺相关病毒,选择性地感染心肌细胞并表达Caren。在用病毒感染心衰模型小鼠后,他们发现,与感染对照病毒的小鼠相比,心肌细胞中的Caren-RNA数量增加,线粒体数量增加,DNA损伤反应的激活受到抑制,从而抑制了小鼠心衰的进展。研究人员还发现,人心肌细胞中存在Caren-RNA,其数量与心力衰竭患者心脏组织中心力衰竭标志基因的表达水平呈负相关(心衰标志基因在低Caren-RNA水平的心脏组织中的表达水平较高。此外,他们还发现,减少人ipS细胞产生的心肌细胞中人Caren RNA的数量会降低线粒体的能量生产能力。
Oike教授说:“我们的研究表明,增加心肌细胞中Caren RNA的数量可以抑制心力衰竭的发生和发展,我们期望这可以成为开发新的心力衰竭治疗方法的策略。在我们的小鼠体内实验中,我们发现使用腺相关病毒的Caren-RNA补充疗法在对抗心力衰竭进展方面是有效的。现在,我们将验证人类Caren是否具有同样的效果,从而开发出一种治疗心力衰竭的新方法。”
这项研究于2021年5月5日发表在《Nature Communications》的网上。
The lncRNA Caren antagonizes heart failure by inactivating DNA damage response and activating mitochondrial biogenesis