数据化冠状病毒疫苗开发指导策略
COVID-19疫苗开发可能需要来自癌症研究的灵感。病毒和癌症有着共同的行为,因此,疫苗开发人员和癌症研究人员应该识别和开发具有跨学科潜力的概念和方法。
例如,费城儿童医院(CHOp)的癌症研究人员开发的一种计算工具已经被用来识别SARS-CoV-2病毒中易受新疫苗攻击的区域。最初,该工具用于识别神经母细胞瘤中的高度特异性生物靶点,从而为工程T细胞的发展提供信息。
这个工具是由医学博士John M.Maris实验室的研究员Mark Yarmarkovich博士开发和改进的,它根据病毒刺激持久免疫反应的能力来确定病毒靶标的优先顺序。最理想的靶标是绝大多数人口中的那些。
在一篇发表在《Cell Reports Medicine》的论文中,Maris团队描述了该工具是如何被用于识别SARS-CoV-2病毒的靶向区域,来设计疫苗靶点的。这篇论文的题目是“Identification of SARS-CoV-2 Vaccine Epitopes predicted to Induce Long-term population-Scale Immunity”,它提出了一种疫苗概念,针对SARS-CoV-2的特定脆弱性,为绝大多数人提供强有力的适应性免疫反应。
为了增加疫苗既安全又有效的可能性,研究人员寻找了SARS-CoV-2的区域,该区域可以刺激记忆性T细胞反应,当与正确的B细胞配对时,将驱动记忆性B细胞的形成,并提供持久的免疫,并适合大多数人类基因组。研究人员瞄准了存在于多个相关冠状病毒中的SARS-CoV-2区域,以及增加传染性的新突变,同时也确保这些区域与人类自然发生的序列尽可能不同,以最大限度地提高安全性。
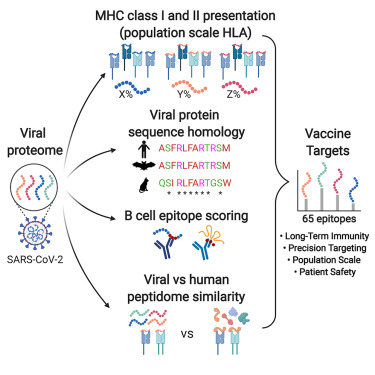
文章作者写道:“在这里,我们提出了一种基于病毒基因组高度保守区域的识别和新获得的适应的SARS-CoV-2疫苗设计概念,这两种疫苗都预计会在绝大多数人群中产生MHCⅠ和Ⅱ类抗原表位。”
“我们提出了一个包含65个肽序列的集合,包含在棘突蛋白进化分化区域内的肽,其中一个子集可以用DNA或mRNA传递策略进行检测。这些肽通过增加与ACE2受体的结合而增加感染性,还包含被认为可以增加膜融合的新进化的furin裂解位点。”
现在,根据研究人员提出的这个包含65个肽序列的清单,当这些肽序列被靶向时,可提供最大概率的群体规模免疫,他们已经开始在小鼠模型中测试十几个这样的序列的各种组合,以评估它们的安全性和有效性。
COVID-19的大流行导致迫切需要开发一种安全有效的疫苗来预防SARS-CoV-2。优化设计的疫苗能最大限度地延长免疫应答,同时最大限度地减少不良反应、自身免疫或疾病恶化。
Yarmarkovich说:“随着过去20年来冠状病毒的第三次流行,这些病毒将继续威胁人类,因此有必要采取预防措施,防止今后爆发疫情。在我们的研究中选择的一部分序列来自与其他冠状病毒非常相似的病毒区域,因此,如果我们的方法成功,不仅可以预防SARS-CoV-2,还可以预防将来可能出现的其他冠状病毒。”
原文检索:Identification of SARS-CoV-2 Vaccine Epitopes predicted to Induce Long-term population-Scale Immunity
(生物通:伍松)