《Nature》美国先进X射线资源挖掘最有希望的COVID-19中和抗体
在全球科竞赛式开发抗SARS-CoV-2疫苗之际,由Vir生物技术公司(Vir Biotechnology)的Davide Corti和华盛顿大学的David Veesler领导的一个国际团队也在24小时昼夜不停地研究一种互补的方法-识别中和抗体,这种抗体可以被用作预防性治疗或暴露后治疗。
他们在伯克利国家实验室(Berkeley Lab)的先进光源(ALS)收集的数据,表明来自SARS幸存者的抗体可以潜在地阻止SARS-CoV-2和其他密切相关的冠状病毒进入宿主细胞。在本周发表在《Nature》杂志上的一项研究中,科学家们指出,最有希望的候选抗体已经在加速临床试验的路上了。
Veesler说:“我们非常兴奋地发现了这种有效的中和抗体,我们希望它能为中止COVID-19大流行出力。”
中和抗体是能与病原体用来感染宿主细胞的一种或多种分子结合而抑制病原体的小蛋白质。在人类和其他动物身上,特殊的免疫细胞会产生中和抗体以应对感染,这样,如果再次遇到同样的病原体,身体就能更快地消灭它。尽管自然中和抗体通常只在最初感染后的有限时间内产生(过去对冠状病毒的研究显示中和抗体能持续一到两年),但科学家只要知道蛋白质序列,就可以制造出相同的抗体。然后,大量生产的抗体可以给那些还没有自身抗体的人。另一方面,有些疫苗也是通过引入一种精心挑选的病原体部分(通常是来自其外表面的分子)或整个病原体的一种减弱或惰性的形式,诱导机体产生自身抗体。
2019年底SARS-CoV-2出现后不久,Veesler和他的同事开始从2003年SARS和2013年MERS的幸存者身上检测潜在的中和抗体。Veesler的结构生物学团队专门研究病原体用来感染宿主的蛋白质机制。这项工作对于发现哪些分子可以成为治疗和疫苗的靶点至关重要。他们先前对引起冠状病毒的SARS和MERS的研究表明,一些中和抗体对这些疾病的反应同样有效。因此,他们怀疑有几种也许能抑制与SARS-CoV密切相关的SARS-CoV-2。
透射电子显微镜下,表面遍布密密麻麻棘突蛋白的SARS-CoV-2病毒
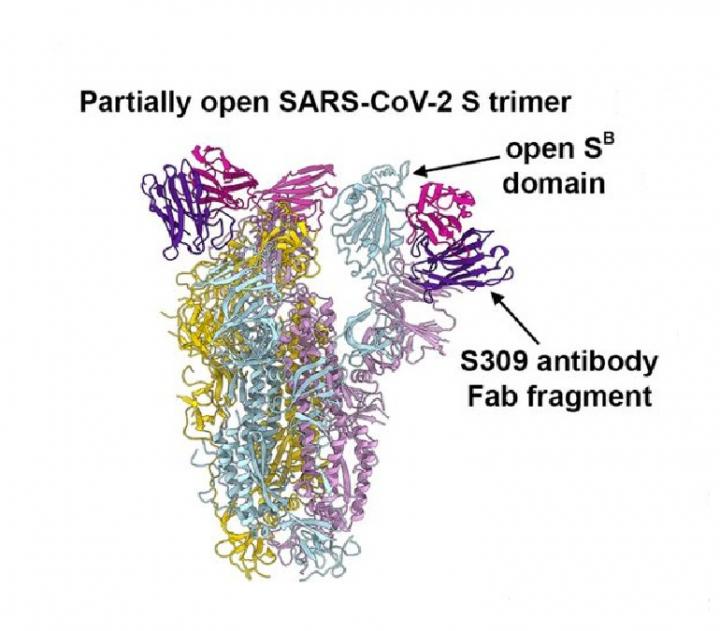
他们筛选出8种能与SARS-CoV-2棘突(spike)糖蛋白结合的抗体。多项研究表明,棘突糖蛋白是中和抗体和疫苗的主要靶点,目前正在开发的疫苗都使用了这种结构的一部分来启动免疫系统。进一步测试缩小了范围,最终发现了一种成功中和SARS-CoV-2的SARS-CoV抗体——S309。
绘制结构图
为了了解这种抗体如何阻碍棘突蛋白,并收集必要的信息来复制它,该研究团队使用华盛顿大学阿诺德分校和梅贝尔贝克曼低温中心的低温电子显微镜(cryo EM)和由伯克利结构生物学中心(BCSB)管理的ALS beamline 5.0.2 X射线晶体学。ALS是一款粒子加速器,它能产生从红外线到X射线的非常明亮的光束。光束被导入同步加速器,以支持广泛的科学技术,包括蛋白质晶体学。
伯克利实验室生物科学部门的生物物理学家、BCSB负责人Marc Allaire说:“David团队是ALS的最新用户。2018年,他们利用ALS检测其他冠状病毒的棘突糖蛋白,并研究潜在抗体如何与它们结合,当发现SARS-CoV-2是一个威胁时,我们能够给研究小组优先安排时间使用。于是,研究小组在2月初和3月31日使用了ALS,分析了S309的结晶样品。
“我在这个领域已经有很长一段时间了,我仍然对蛋白质结晶学的力量着迷,”Allaire补充说。在结晶学中,一束X射线瞄准结晶的样品产生衍射图样。然后测量衍射点的强度,并用于重建分子原子结构的三维图。Beamline 5.0.2是一种专门的晶体学粒子加速器,已运行20年,支持广泛的结构生物学研究和药物发现。“我们很荣幸能为S309的发现做出贡献。”
原文检索:Cross-neutralization of SARS-CoV-2 by a human monoclonal SARS-CoV antibody
(生物通:伍松)