WB实验总做不好,那么如何进行WB实验质控呢?
做过WB实验的小伙伴都经历过成像时忐忑不安,出来结果时的彷徨无措,为什么条带没有出啦,为什么背景这么高,为什么受伤的总是我,看着旁边小伙伴漂亮的结果图,心生羡慕嫉妒,那么小编给大家整理总结了如何进行WB的质控和注意哪些检查点。
蛋白样品:准备好裂解液后,使用BCA或Bradford等检测方法仔细测量蛋白浓度。进行上样时,确保加入等量的蛋白样品,以确保公平比较,从而最大限度地减少上样误差。不要使凝胶过载! 如果您的表达目标非常低,可选择加样孔体积大的凝胶,这样可提高上样量。
阳性和阴性对照:这些质控对于证明您的结果有效至关重要。 阳性对照通常是裂解物或组织提取物,其具有过度表达的蛋白。当您的阳性对照未能发出信号时,您知道该方法可能存在问题。如果您正在使用重组蛋白,那么包含内源形式靶标的阳性对照也是一个好主意。这将有助于理清与一抗相关的任何特异性问题。阴性对照同样也有价值,通常是不会产生目标的裂解物或组织提取物。 最好的阴性对照由敲除或未处理的细胞系制备。
内参对照:有几种广泛可用的上样对照抗体,如GApDH、actin 或 tubulin。 由于这些蛋白表达丰度高,因此在适应低丰度目标的样品表达看到内参对照蛋白的过饱非常常见。 这里最大的挑战是内参对照和靶蛋白在相同的样品稀释系列中通常具有不同的线性,影响定量的准确性,对于目的蛋白表达比较低的蛋白,可选择低表达的内参例如Lamin B1和HSp60等蛋白。 此外,研究人员需要证明内参蛋白的表达不会因实验条件的变化而改变。
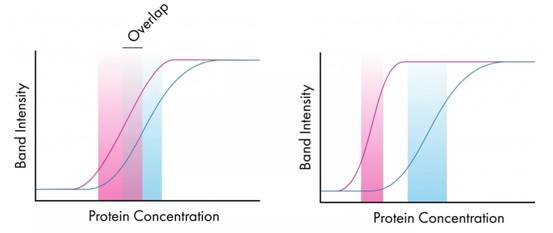
在第一个检测线性范围重叠的地方,蛋白质在该重叠区域内的定量将是很好的。 然而,在后者中,它们不重叠,容易看出蛋白质浓度的变化如何影响一种蛋白条带强度,而不影响另一种蛋白质的条带强度。 在这种情况下,定量是不准确的。
转移效率/总蛋白标准化:转印完成后,最好评估转移到膜上的蛋白量以及凝胶中剩余的蛋白量。通过评估整个蛋白范围,产生更广泛的动态范围。 这些染色包括凝胶和膜染色,并且可以以各种不同的方式成像。例如AzureRed荧光蛋白染色是一种用于凝胶和印迹膜的定量总蛋白染色试剂,与下游蛋白分析兼容。 AzureRed是染色应用的理想选择,包括转印后染色以确认从凝胶到膜的蛋白质转移情况,以及定量蛋白。执行这些检查不仅可以让您对实验的进展充满信心,现在很多期刊杂志都推荐使用总蛋白定量的方法来进行质控,以证明数据的可重复性和准确性。
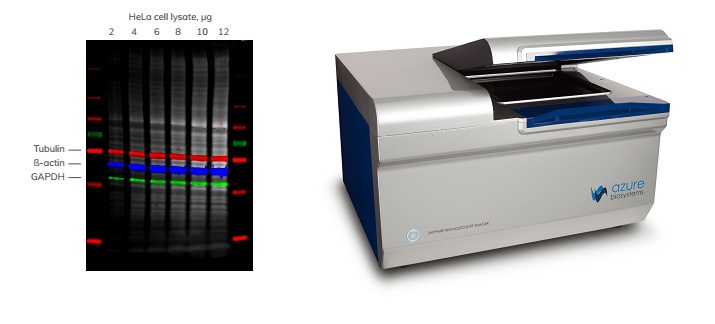
图1. AzureRed与三种感兴趣的蛋白同时成像。
向凝胶中加入稀释的HeLa细胞裂解物。转印后,将印迹用AzureRed染色,然后在不脱色情况下加入tubulin、ß-actin和GApDH探针。用Azure Sapphire 双模式多光谱激光成像系统扫描成像。四个通道进行叠加,总蛋白质(AzureRed染色)以灰色显示;tubulin-红色,ß-actin-蓝色和GApDH-绿色。
不加入一抗:这是一个简单但经常被遗忘的WB印迹控制。通过仅仅加入二抗孵育印迹,您将能够清楚地看到由于实验中使用的二抗而产生非特异性的条带。
通过小编的介绍,做好质控,相信您的WB数据也是妥妥的。
联系我们:
北京深蓝云生物科技有限公司
地址:北京市北京经济技术开发区经海四路25号院2号楼2单元2层201室
电话:010-57256059
邮箱:[email protected]
官网:www.cycloudbio.com