Leukemia:阻断NF-κB信号,找到急性淋巴细胞白血病耐药复发潜在治疗靶点
儿童急性淋巴细胞白血病(ALL)是儿童最常见恶性肿瘤之一,现阶段我国儿童ALL的治愈率约为70%(国际最高治愈率约为80%)。患者对相关治疗药物的耐药性以及由此引起的复发是治愈率难以提升的瓶颈。因此,如何破解儿童白血病耐药复发及其克隆演化机制已成为这一领域的研究焦点。
上海交通大学医学院附属上海儿童医学中心、国家儿童医学中心的研究人员发表了题为“Blocking ATM-dependent NF-κB pathway overcomes niche protection and improves chemotherapy response in acute lymphoblastic leukemia”的文章,率先证实阻断ALL细胞中ATM依赖的NF-κB信号通路能够克服来自骨髓微环境对化疗后微小残留白血病细胞的保护作用,显著提高ALL的化疗效果,对临床后期开展ALL联合治疗具有重要意义。
这一研究成果公布在血液学国际权威学术杂志Leukemia(《白血病》,影响因子10.023)上,文章通讯作者分别为上海儿童医学中心儿科转化医学研究所所长周斌兵教授,上海儿童医学中心儿科转化医学研究所段才闻副研究员和上海市转化医学协同创新中心主任陈红专教授。
背景
ALL是儿童最常见恶性肿瘤之一,也是所有儿童疾病中造成死亡的主要原因。通过风险分层组合化疗和改善支持治疗,ALL患者的5年生存率已达到80%以上。然而,近20%的患者仍然会复发,导致治疗失败。因此必须进行ALL复发综合机制研究,制定克服耐药性和ALL复发的治疗策略。
一系列研究表明遗传突变会导致儿童ALL的复发。科学家们通过基因谱分析和测序确定了几种复发特异性耐药突变,同时也提出残留耐药细胞可以在化疗中存活,然后随后利用获得性抗药性来推动克隆进化,导致白血病快速增殖。然而,剩余的ALL细胞在化疗中所处的位置及其存活机制,尚不清楚。 越来越明显的是,白血病细胞与其微环境(或生态位)之间的相互作用在疾病复发过程中起着重要作用。
骨髓(BM)微环境是一个复杂且良好调节的微环境,由非造血基质细胞,细胞外基质和细胞因子组成。它调节造血干细胞(HSCs)的稳态,并参与ALL的发病机制和耐药性。(研究中使用的人骨髓间充质干细胞无血清培养基来自赛业生物)
找文献同款热门产品?点我咨询
重要发现
上海交通大学医学院附属上海儿童医学中心的研究人员此前曾发现通过化疗后ALL细胞分泌的细胞因子会召集BM细胞,重建了一个不断发育的环境,来保护残留ALL细胞。这种细胞因子,即GDF15,CCL3和CCL4,在ALL进展中起重要作用。然而,这些细胞因子如何通过化疗诱导,仍然未知。
在最新这项研究中,研究组发现化疗引起ALL细胞基因损伤应答(DDR)和NF-κB信号通路激活,其中DDR关键蛋白ATM结合并激活泛素化连接酶TRAF6,导致NF-κB组份IκB降解,进而使NF-κB核心组份p65蛋白释放入核,促进其直接下游细胞因子GDF15,CCL3和CCL4的表达和分泌增加,在骨髓中形成保护残留白血病细胞的微环境,促进导致复发微小残留白血病细胞的生存,为ALL耐药复发突变的获得奠定了基础。
与此同时,研究人员还利用ATM和p65特异性小分子抑制剂体内阻断ATM依赖的NF-κB信号通路,联合临床一线化疗药物,显著减少微小残留白血病细胞并提高ALL的化疗效果。
这一研究成果阐明了ALL复发前期起始克隆产生的机制,揭示了克服ALL耐药复发潜在的治疗靶点,为进一步提高我国儿童ALL治愈率奠定坚实的理论基础。
国际血液病权威专家、哥伦比亚大学癌症遗传研究所Adolfo Ferrando教授高度肯定此项研究成果,他认为,ALL的耐药复发是世界性难题,阻断ATM依赖的NF-κB信号通路提高ALL化疗效果具有非常重要的临床转化和治疗意义。
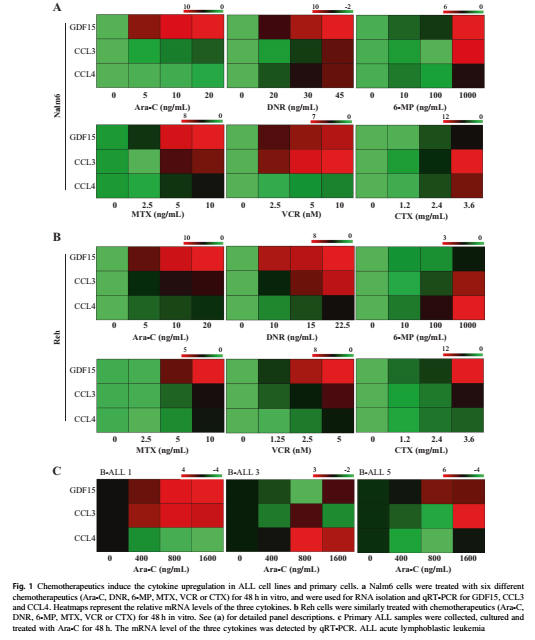
化疗引起ALL细胞系和原代细胞中的细胞因子上调
研究人员以前曾发现ALL保护微环境由细胞因子(GDF15,CCL3和CCL4)重建,这些细胞因子经Cytrarabine(Ara-C)处理后会上调。
为了确定化疗诱导这些细胞因子的机制,他们用化疗药物Ara-C,柔红霉素(DNR),巯嘌呤(6-Mp),甲氨蝶呤(MTX),长春新碱(VCR),CTX和地塞米松(DEX)治疗了两种ALL细胞系(Nalm6和Reh),然后通过qRT-pCR测定细胞因子的表达水平。
如上图所示,Nalm6和Reh细胞中GDF15,CCL3和CCL4的mRNA水平以药物剂量依赖性方式显著增加。在实验的不同化学治疗剂中,Ara-C,DNR和6-Mp引起了直接DNA损伤和最显著的细胞因子上调,因此用于进一步研究。
为了补充mRNA水平检测,在用Ara-C,DNR和6-Mp处理后,研究人员通过ELISA在Nalm6和Reh细胞中测定了三种细胞因子的分泌蛋白水平。结果显示,Nalm6和Reh细胞中三种细胞因子的蛋白质水平以剂量依赖性方式显著增加(图S1C和D)。因此研究人员认为化疗药物,特别是DNA损伤剂,可以在不存在BM微环境的情况下直接诱导ALL细胞中的趋化因子产生。在化疗处理的ALL细胞系和原代细胞中,微环境保护相关细胞因子的表达水平增加。
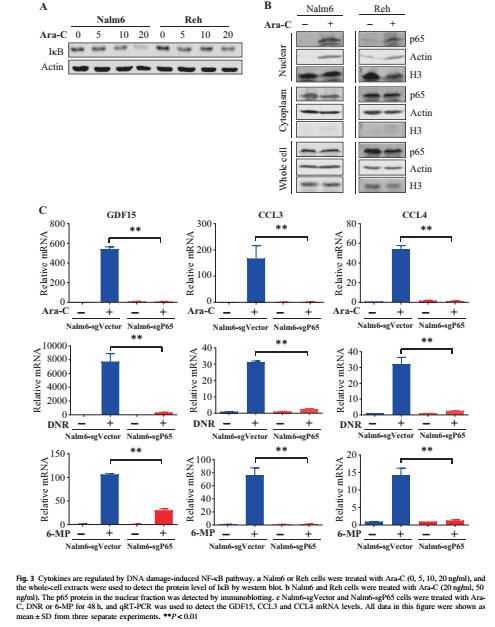
化疗后NF-κB通路被激活
转录因子NF-κB在应激条件下能调节细胞因子,如CXCL10和IL6的产生,因此在肿瘤侵袭和炎症反应中起关键作用。
在最新这项研究中,研究人员发现NF-βB途径可能调节参与微环境保护细胞因子的表达。他们发现了经过Ara-C处理后,IκB蛋白水平会降低(图3a),NF-κB组分之一——p65,在Nalm6和Reh细胞中易位到细胞核中(图3b;图S5A)。
这一结果表明NF-κB途径经Ara-C处理后激活。为了研究NF-κB途径与细胞因子上调之间的因果关系,研究人员使用CRISpR/Cas9方法构建p65敲低细胞系(Nalm6-sgp65和Reh-sgp65)(图S5B和C),发现在Ara-C,DNR或6-Mp处理后,p65中的细胞因子显著减少了(图3c;图S5D)。而且NF-κB抑制剂pDTC阻断p65易位进入细胞核(图S5A),抑制细胞因子表达(图S5E),从而支持NF-κB途径被激活并参与体外调节GDF15,CCL3和CCL4的表达。
想了解更多稳转细胞系应用案例?点我咨询
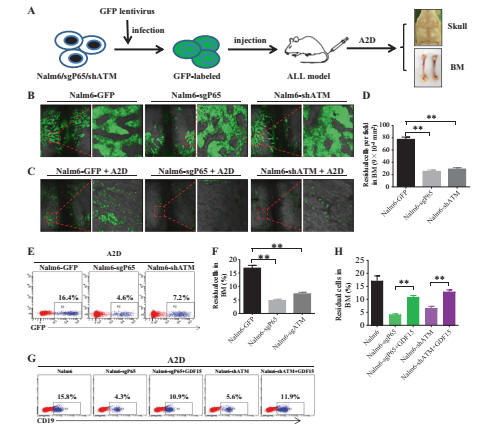
阻断NF-κB途径增强了ALL细胞对化学疗法的敏感性
研究人员还分析Nalm6和Reh ALL小鼠模型中阻断ATM依赖性NF-κB途径的化学敏感性。用Ara-C处理2天后,杀死小鼠并通过离体荧光共聚焦成像和FAC从颅骨和BM中检测到GFp+ ALL细胞(图6a)。
如图6b所示,Nalm6-GFp,Nalm6-sgp65-GFp和Nalm6-shATM-GFp细胞在化学疗法之前将整个血管浸入颅骨中。化疗后Nalm6-sgp65-GFp和Nalm6-shATM-GFp小鼠头骨中残余GFp + ALL细胞的数量显著低于Nalm6-GFp小鼠(图6c,d)。同时,超过10%的GFp+ ALL细胞保留在Nalm6-GFp小鼠的BM中,而少于5%的GFp+ ALL细胞保留在Nalm6-sgp65-GFp和Nalm6-shATM-GFp小鼠(图6e,f)。
这些结果表明,在体内阻断ATM依赖性NF-κB活化后,Nalm6细胞对Ara-C的敏感性提高。在Reh ALL异种移植模型中获得了类似的数据(图S10A-E)。
由于GDF15阻断抗体可以抑制ALL微环境,因此研究人员认为添加外源GDF15可以逆转阻断ATM依赖性NF-κB通路的体内效应。为了验证这一假设,他们确定了p65和ATM敲低ALL模型对化疗的敏感性是否可以通过外源性添加GDF15来逆转。结果显示残留的白血病细胞明显增加了GDF15预处理后,Ara-C处理的Nalm6-shATM和Nalm6-sgp65(图6g,h)。
免费索取基因编辑小鼠模型设计方案
这一研究成果阐明了ALL复发前期起始克隆产生的机制,揭示了克服ALL耐药复发潜在的治疗靶点,为进一步提高我国儿童ALL治愈率奠定坚实的理论基础。
国际血液病权威专家、哥伦比亚大学癌症遗传研究所Adolfo Ferrando教授高度肯定此项研究成果,他认为,ALL的耐药复发是世界性难题,阻断ATM依赖的NF-κB信号通路提高ALL化疗效果具有非常重要的临床转化和治疗意义。
原文标题:
Blocking ATM-dependent NF-κB pathway overcomes niche protection and improves chemotherapy response in acute lymphoblastic leukemia
https://www.nature.com/articles/s41375-019-0458-0