反义寡核苷酸疗法穿过血脑屏障
2021年8 月 13 日——研究人员已经证明,与胆固醇结合的异源双链寡核苷酸药物可有效穿过血脑屏障,可用于治疗中枢神经系统 (CNS) 疾病。该研究结果于 8 月 12 日发表在Nature Biotechnology上。
反义寡核苷酸 (ASO) 治疗剂是包含 18 到 30 个碱基对的分子,可修饰目标 mRNA 的表达,目的是抑制有害蛋白质或非编码 RNA。这些碱基对以反向(反义)排列,并通过与 mRNA 靶标的“有义”链结合来阻止致病蛋白的产生。
一般来说,只有分子量小于450道尔顿的疏水小分子才能穿透血脑屏障和血脑脊液屏障。ASOs 是高度极性的,因此在系统给药后通常不会完整地进入大脑。
东京医科齿科大学、武田制药和 Ionis 制药的研究人员开发了与胆固醇 (Chol-HDO) 或 α-生育酚 (Toc-HDO) 结合的 DNA/RNA 异源双链寡核苷酸 (HDO) 作为药物递送平台。他们希望该技术能够克服 ASO 靶向 CNS 的有限功效,而无需鞘内给药。
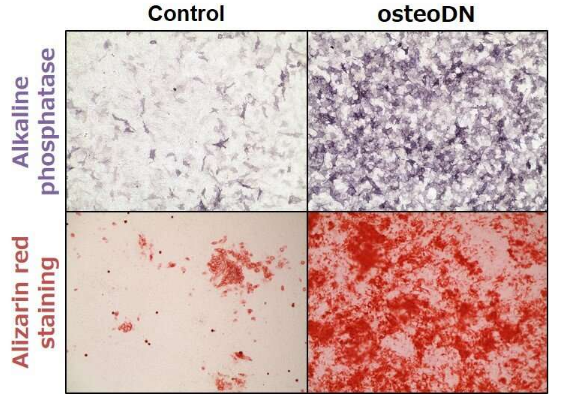
科学家们合成并评估了 14 种亲脂性偶联物,包括 9 种天然脂肪酸和甾醇,用于小鼠中枢神经系统的基因敲除。单链 ASO 和脂质偶联的 HDO 以 50 mg/kg 的剂量静脉注射。通过定量聚合酶链反应 (PCR) 和逆转录 (qRT-PCR) 在大脑皮层中测量靶基因表达水平——转移相关的肺腺癌转录物 1 (Malat1) RNA。
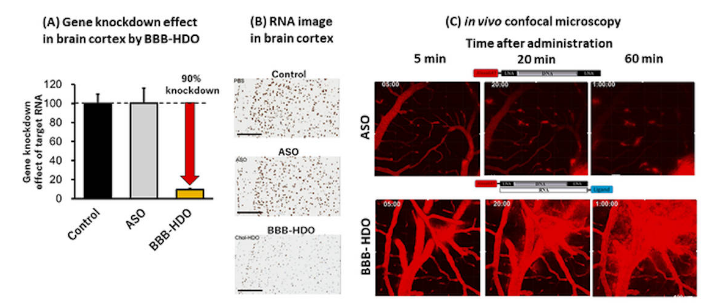
研究小组发现,HDO 分布在整个大脑、脊髓和外周组织中,可将中枢神经系统中靶基因的表达抑制高达 90%,而与胆固醇结合的单链 ASO 的活性有限。
第一作者、东京医科牙科大学副教授 Tetsuya Nagata 博士说:“我们发现,与胆固醇-ASO 不同,胆固醇结合的 HDO(Chol-HDO)在实验动物皮下或静脉内给药后可以有效地到达 CNS,”在一份声明中。“Chol-HDO 平台显示出显着的剂量依赖性靶基因减少,并在所有 CNS 区域和细胞类型中发挥长期作用。”
此外,长链脂肪酸结合物——月桂酰 (C12)、月桂酰 (C12OH)、硬脂酰 (C18) 和 α-生育酚——显示出中枢神经系统中 Malat1 的适度抑制,但胆固醇结合物是最有效的,单次静脉注射可将 Malat1 水平降低约 60%。作者认为,具有环状结构框架的胆固醇和生育酚比直链脂肪酸更有效。
他们还研究了多次注射以及皮下给药的药代动力学。在体内,反复注射 Chol-HDO 使中枢神经系统中的 Malat1 减少了约 90%,使用 Toc-HDO 观察到的减少了大约 50%。Chol-HDO 的这种 RNA 减少在整个大脑中持续了两个多月。小鼠的结果也在大鼠模型中得到证实。