建立脑肿瘤环境的三维模型有助于个体化治疗
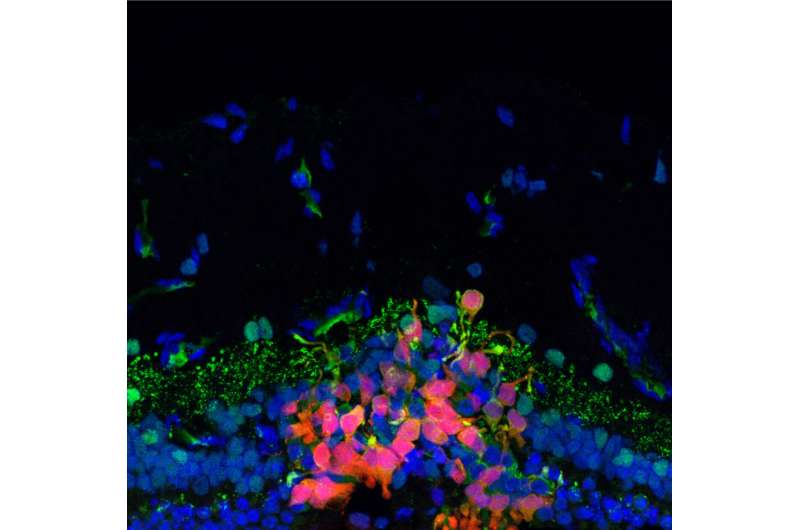
图:加布里埃拉·门德斯(Gabriela Mendes)是VTC Fralin生物医学研究所的博士后助理,他拿着一个胶质母细胞瘤肿瘤微环境的3D模型,该实验室开发了这个模型来研究不同人的癌症对不同疗法的反应。
图片来源:Clayton Metz for Virginia Tech
胶质母细胞瘤是一种罕见但致命的脑癌,非常顽固。外科医生切除肿瘤后,却只能看到恶性复发。化疗和放疗效果有限。大约一半的患者在18个月内死亡。
但是现在弗吉尼亚理工大学的科学家们开发了一种新的胶质母细胞瘤肿瘤微环境的3D组织工程模型,可以用来研究肿瘤复发的原因,以及根除它们的最有效的治疗方法——直接到病人的特定水平。
7月29日发表的一篇论文描述了该模型及其发展
“我们的最终目标是开发一种个性化的医疗方法,我们可以取病人的肿瘤,在培养皿中建立肿瘤模型,在上面测试药物,并告诉临床医生哪种治疗方法最有效,”VTC的弗拉林生物医学研究所副教授、该论文的通讯作者詹妮弗·曼森(Jennifer Munson)说。
该模型是识别新的癌症标志物和治疗方法的重要一步。使用新模型的研究已经确定了一种了解患者肿瘤的新方法,包括癌细胞自我更新和分化的能力,这是癌症对药物治疗的反应的一个指标。
根据美国国家癌症研究所(National Cancer Institute)的数据,每年约有1.5万人被诊断出患有胶质母细胞瘤。
曼森是一名组织工程师,也是弗吉尼亚理工大学生物医学工程与力学系的副教授,也是弗吉尼亚理工大学癌症研究联盟的联合主任之一。他于2014年开始开发这种模型。虽然存在其他工程模型,但这一模型考虑了肿瘤细胞以外的细胞类型,以及肿瘤生长和扩散的空间,以及实际肿瘤微环境的其他方面。
曼森的模型通常只有铅笔橡皮擦大小,更准确地再现了研究的环境,包括中枢神经系统特有的细胞,如星形胶质细胞和小胶质细胞,其比例也基于患者身上发现的细胞。
该模型还考虑了组织中细胞间和细胞周围的液体流动,即所谓的间质液体流动,这种流动在肿瘤中会增加,并加速癌症的扩散。模型中的流体流动也可以方便地进行药物治疗的测试。
微环境对于理解为什么胶质母细胞瘤如此难以治疗至关重要。虽然肿瘤可以被切除,但肿瘤细胞倾向于侵入周围的组织,在那里它们变得更有害或对治疗更有抵抗力,让癌症复发。
曼森说:“我们想要尽可能地模拟那种环境,因为那是你以后使用药物或进行任何后续治疗的情况。”
曼森和她的团队使用这些模型来测试不同治疗方法的影响,分析癌细胞如何入侵组织,它们如何增殖,它们的自我更新能力,以及有多少细胞死亡。他们发现结果差异很大,这凸显了对胶质母细胞瘤进行个性化治疗的重要性,以及能够重建个体患者肿瘤微环境的价值。
“这个模型可以帮助我们回答一些问题,比如我们能否预测治疗反应?”老李说。“我们能否看到这些不同类型的细胞如何影响肿瘤细胞的行为,或者我们能否更好地了解这种微环境,让医生更有效地治疗那些生存机会通常很低的患者?”