Cell:首例临床用噬菌体成功清除耐药性脓肿分枝杆菌肺部感染!
用病毒杀死细菌似乎是医学上的倒退,让人想起20世纪初,Julius Wagner-Juarreg利用疟疾治疗神经梅毒——这一壮举让他获得了诺贝尔奖。然而,噬菌体已经进化到可以攻击特定的细菌。近年来,研究人员发现了新的野生型噬菌体菌株和分子机制,使研究人员能够设计噬菌体病毒针对特定细菌。
现在,研究人员首次成功地使用噬菌体治疗一种耐抗生素的分枝杆菌肺部感染,为囊性纤维化的年轻患者接受救命的肺部移植扫清了道路。Cell杂志上发表了一篇题为《Host and pathogen response to bacteriophage engineered against Mycobacterium abscessus lung infection》的案例研究,报道了噬菌体治疗脓肿分枝杆菌肺部感染的成功应用。
背景
噬菌体是选择性感染细菌并可以裂解复制导致细菌死亡的病毒。越来越多的溶菌噬菌体被评估用于治疗难治性感染。脓肿分枝杆菌( M. abscessus ) 是一种非结核分枝杆菌 (NTM),具有高水平的内在和获得性抗生素耐药性,限制了治疗选择并导致不良结果。脓肿分枝杆菌被认为是噬菌体治疗的潜在重要靶标。
囊性纤维化 (pwCF) 患者易患 NTM 肺病。脓肿分枝杆菌感染与肺功能更严重的下降有关。治疗难治性肺移植有禁忌症。在晚期 CF 肺病中,脓肿分枝杆菌感染的抗生素治疗可能不成功,因为肺的结构变化,特别是空腔和致密实变和实质塌陷区域,这限制了抗菌药物的治疗浓度。已知脓肿分枝杆菌在 CF 气道内形成生物膜,在受损肺内的微环境中,分枝杆菌可能会在没有氧气或营养的情况下存活很长时间,因为它会转变为一种非复制的“持久”状态,这可能会进一步阻碍传统的抗菌剂和宿主防御。
脓肿分枝杆菌临床分离株的噬菌体敏感性差异很大,因此需要针对每个患者个性化治疗性噬菌体。大多数感染脓肿分枝杆菌的噬菌体是温和的整合型,必须经过工程改造,使其对脓肿分枝杆菌具有裂解性而不是溶原的行为。作者还提出需要考虑针对噬菌体的抗体影响,出现耐噬菌体的菌株,以及如果用噬菌体大量杀死脓肿分枝杆菌而空出来的生态位被其他病原体占据的情况。
晚期 CF 肺病中难治性脓肿分枝杆菌感染的临床表现
该患者是一名 26 岁男性,患有 CF(基因型 H199Y/2184insA),当他还是个孩子的时候,他每年都要进好几次医院。成年后经历了持续6年脓肿分枝杆菌感染后肺功能迅速下降,患有晚期支气管扩张、脓肿分枝杆菌肺病,以及耐多药 (MDR)铜绿假单胞菌和耐甲氧西林金黄色葡萄球菌的慢性肺部感染。他的临床病程以频繁的肺部恶化而著称,需要住院和静脉注射 (iv) 抗生素治疗。他一直服用 4 到 5 种药物,这些药物根据药物可用性、敏感性测试、副作用耐受性和对治疗的反应进行轮换。在他频繁住院期间,治疗脓肿分枝杆菌的药物从未少于四种,另外同时治疗铜绿假单胞菌和 MRSA。
尽管进行了强化治疗,患者的脓肿分枝杆菌亚种脓肿培养持续阳性,影像学特征恶化,肺功能下降,在噬菌体给药前的 12 个月中,他需要 11 次住院,时间从 11 天到 21 天不等。到2020年,他的肺功能下降到了30%以下。医生们认为,如果不进行肺移植,他可能在几年内就会死亡。他被三个独立的肺移植计划拒绝进行肺移植,部分原因是缺乏治疗难治性脓肿分枝杆菌肺病的治疗选择。分枝杆菌可以从肺部扩散到皮肤和其他组织,这可能会使接受移植的患者在接受免疫抑制药物治疗时陷入困境。
同情给药
研究人员对患者感染早期分离的脓肿分枝杆菌全基因组测序,并使用噬菌斑测定筛选对患者样本的脓肿分枝杆菌有感染性的噬菌体,匹兹堡大学生物科学教授Graham Hatfull博士和他的团队筛选了几十个候选噬菌体,并确定了两种噬菌体 BpsΔ 33 HTH_HRM10 和 D29_HRM GD40能有效杀死感染患者肺部的分枝杆菌的噬菌体,被选为治疗性噬菌体混合物。他们对噬菌体进行改造,去除了部分阻遏基因,使之成为裂解噬菌体。经过反复筛选验证,噬菌体被扩增并纯化至高效价且证明是无菌和无内毒素的。
分枝杆菌噬菌体给药的临床反应
噬菌体给药于 2020 年 9 月开始,当时患者因肺部恶化住院期间接近基线临床状态。持续每天 iv 两次给药,耐受性良好,没有归因于治疗的不良事件。他在噬菌体治疗开始后第 5 天出院。在噬菌体治疗启动后的第 5 天和第 362 天之间获得17个NTM 痰培养物,前面7次(治疗5-96天)有6次NTM阳性,后 10 次培养物中的 9 次(第 116-362 天)NTM为阴性(在第 245 天恢复了一个分离株)。相比之下,同期13 个 气道培养物中只有 1 个为铜绿假单胞菌或 MRSA 阴性。基于脓肿分枝杆菌感染得到控制的证据,他在噬菌体治疗开始一年后被列入肺移植名单,并在第 379 天成功移植。
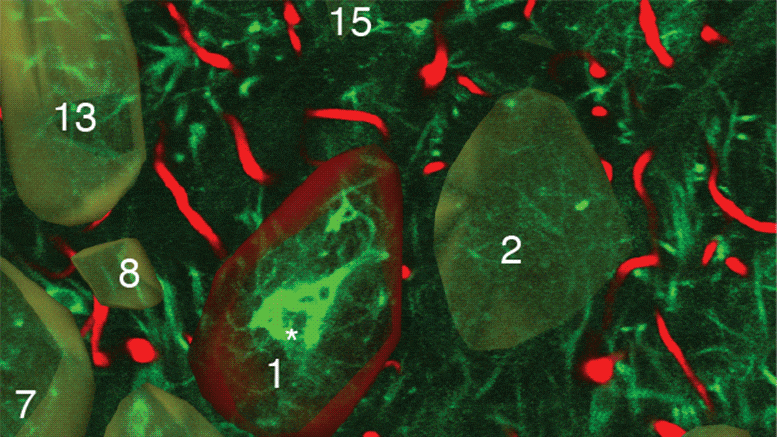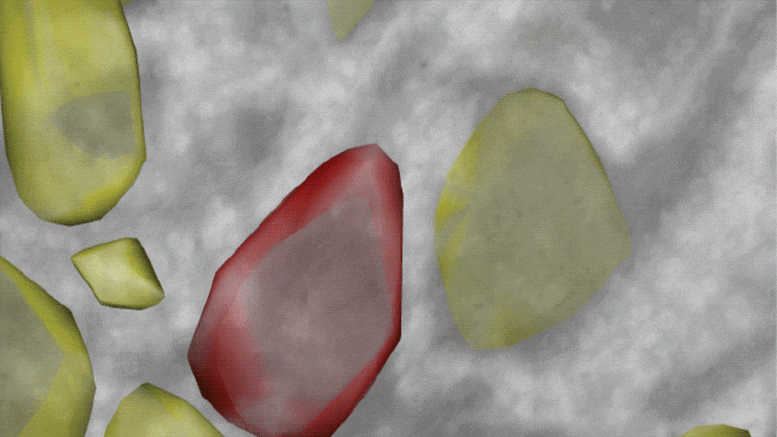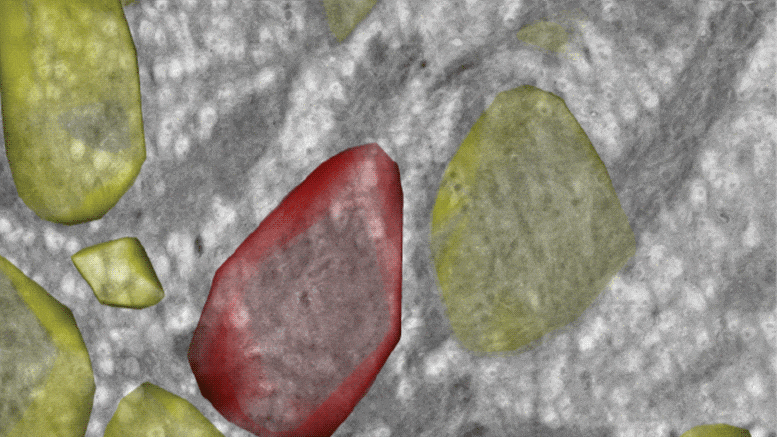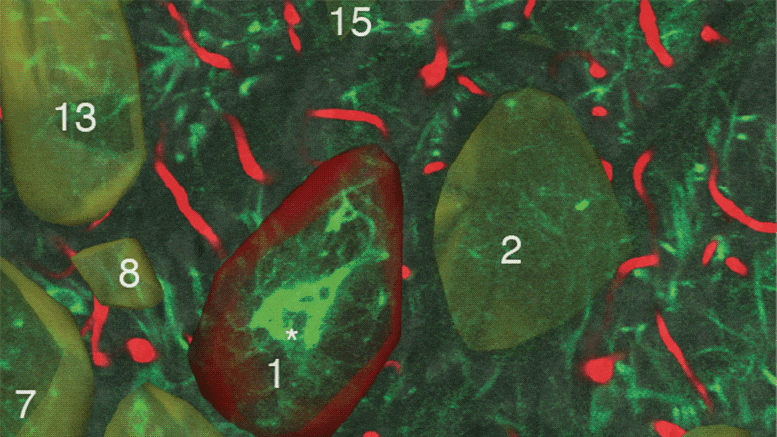
移植肺组织及移植后病程的系统分析
移植时,对患者肺部进行了脓肿分枝杆菌检查。支气管肺泡灌洗液、未处理的支气管内分泌物拭子、来自每个肺叶的均质组织以及主干支气管血管边缘进行酸性杆菌 (AFB) 染色,培养 NTM 和细菌,并通过实时定量 pCR 分析(qpCR)。所有样本类型的 AFB 均呈阴性。所有肺叶和左主支气管 (LMB) 的铜绿假单胞菌培养物均为阳性。虽然通过 qpCR 在支气管肺泡灌洗液和三个肺叶和一个肺叶支气管内分泌物中检测到脓肿分枝杆菌DNA,但所有样本的脓肿分枝杆菌培养没有生长。移植肺的大体病理学未显示肉芽肿。在噬菌体治疗的第 500 天(移植后 121 天)通过支气管肺泡灌洗液对移植肺取样的另外 5 种气道培养物对脓肿分枝杆菌呈阴性,没有播散性感染的临床证据。患者经历了从移植中恢复的简单过程,肺功能正常化,并继续接受噬菌体和抗生素治疗。
“多年来,我们一直试图用各种抗生素清除分枝杆菌感染,但都没有成功,”首席研究员Jerry Nick医学博士解释说,他是国家犹太健康成人囊性纤维化项目的主任。“当我们使用这种细菌自身的天敌时,我们能够清除感染,这导致了肺部移植的成功。”

囊性纤维化是一种遗传性疾病,会导致肺部黏液堆积,导致反复的细菌感染,损害肺部,并可能导致呼吸衰竭。虽然新的治疗方法大大改善了囊性纤维化患者的预后,但预期寿命仍然显著降低。
分枝杆菌是一种常见和广泛分布的细菌属,可导致结核、麻风病和非结核分枝杆菌(NTM)感染。脓肿分枝杆菌是一种特别具有侵袭性和挑战性的NTM感染。多种抗生素联合治疗和一年或更长时间的治疗通常不成功。国家犹太健康中心拥有全国最广泛的成人囊性纤维化项目,是治疗NTM感染的领先中心。
接受肺移植手术的Jarrod Johnson说:“我非常感谢参与我治疗的所有人的努力、坚持和创造力。”“我以为我要死了。他们真的救了我的命。”
“脓肿分枝杆菌经噬菌体处理前后表现出遗传稳定性,多样性普遍下降,对噬菌体或抗生素的耐药性没有增加。对一种噬菌体的抗噬菌体中和抗体滴度随时间增加,但在整个治疗过程中并不妨碍临床改善。”“这项研究可以作为未来使用噬菌体治疗严重脓肿分枝杆菌肺部感染患者和拯救生命的路线图,”Nick总结。