ACS Catalysis|发现一例新型中链酰基辅酶A羧化酶负责聚酮合酶延伸单元合成并应用至聚酮骨架改造
近日,武汉大学药学院邓子新院士团队于《ACS Catalysis》杂志在线发表聚酮合酶延伸单元合成研究与聚酮骨架改造成果。论文以武汉大学为第一署名单位,博士研究生张俊为第一作者,瞿旭东教授与朱冬青副教授为共同通讯作者。
聚酮(polyketide)是一大类结构复杂且具有良好生物活性的天然产物,被广泛应用于医药和农业领域。聚酮多样且优良的药理活性与分子结构密不可分,基于聚酮天然产物的生物合成逻辑,科学家可以通过操作聚酮生物合成过程实现其结构的改造;这其中,延伸单元作为聚酮合成的关键砌块对聚酮骨架的结构多样化至关重要,因此也被认为是改造聚酮碳骨架的最重要的切入点。
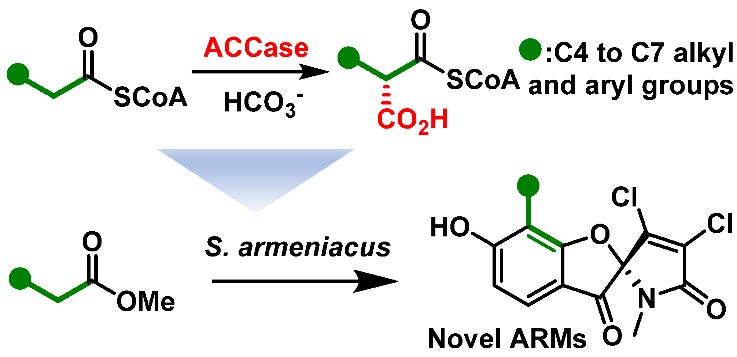
研究人员基于前期朱冬青课题组对来源于链霉菌S. armeniacus DSM 43125的活性聚酮分子armeniaspirol的生物合成分析(J. Nat. prod. 2019, 82, 318),发现了一例新型酰基辅酶A羧化酶β亚基Arm13参与了armeniaspirol骨架中C6位的一个特殊烷基侧链的生物合成。进一步对Arm13研究,发现该β亚基可以与不同来源的α和ε亚基组装成一个具有高度催化活性的羧化酶复合体(ACCase);该羧化酶能够识别各种链长(C4-C10)以及末端带有烯基、炔基、卤素、苯环、吲哚等各种官能团的酰基辅酶A(acyl-CoA)底物,并将其高效转化成相应的丙二酰单酰辅酶A类型的延伸单元。基于ACCase强大的合成延伸单元的能力,研究人员通过向armeniaspirol产生菌中喂养简单的羧酸甲酯底物,成功的在armeniaspirol骨架的C6位引入了烯基、炔基以及苯环等一系列活泼官能团,证实了该羧化酶在聚酮延伸单元的合成以及碳骨架的编辑方面的巨大潜力。
本研究为聚酮延伸单元的合成,以及聚酮碳骨架的理性改造与结构多样化提供了强有力的工具酶和研究思路。
该研究获得国家重点研发计划项目与国家自然科学基金项目支持。
论文链接:A permissive Medium Chain Acyl-CoA Carboxylase Enables the Efficient Biosynthesis of Extender Units for Engineering polyketide Carbon Scaffolds | ACS Catalysis






























