有意思!疟原虫是如何“滑”进人体的?
滑行这个动作是顶复门的寄生虫所特有的,比如疟原虫和弓形虫。这两种寄生虫通过蚊子和猫传播,对全球人类健康产生了巨大影响。疟原虫导致2.28亿人感染疟疾,且每年大约有40万人死亡。弓形虫可能在女性怀孕期间影响胎儿健康。
这些寄生虫通过滑行进入宿主细胞,并在宿主细胞之间移动。例如,疟原虫通过蚊虫叮咬的部位进入人体,然后再进入人体血管。这种独特的运动形式依赖于肌动蛋白(actin)和肌球蛋白(myosin)。肌球蛋白的分子“腿”沿着肌动蛋白丝前进,从而产生运动。
肌球蛋白还与其他几种蛋白质相互作用,组装成一种复合物,名为滑行体(glideosome)。由于大多数滑行体蛋白质的结构未知,人们目前还不大了解滑行体是如何起作用的。然而,了解这种机制有助于开发防止滑行体组装的药物,从而阻止疟疾和弓形体病等疾病的发展。
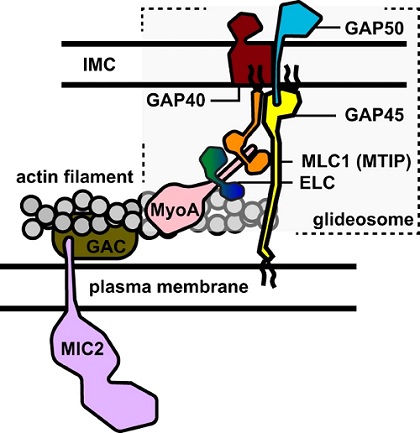
滑行体结构的示意图(来自原文)
欧洲分子生物学实验室的研究人员近日分析了滑行体中的必要轻链(ELC)的分子结构,这些蛋白质与肌球蛋白直接结合。它们是滑行所必需的,不过确切结构和功能还未知。研究人员通过X射线晶体学和核磁共振(NMR)获得了刚地弓形虫和恶性疟原虫的ELC分子结构。
这项研究成果发表在《Communications Biology》杂志上,表明ELC的作用有些类似“分子高跷”。一旦与肌球蛋白A(MyoA)结合,ELC变得僵硬,并开始充当其杠杆臂。这种硬化使得肌球蛋白能够前进更长的距离,这可能会加速寄生虫的滑行运动。
他们还研究了钙在ELC与肌球蛋白A之间的相互作用中扮演什么角色。令人惊讶的是,他们发现钙并不影响ELC的结构。不过,它确实增加了ELC-肌球蛋白A复合物的稳定性。该结果表明,滑行体的结构中还隐藏着许多的未知数。
EMBL研究人员Matthew Bowler表示:“这项工作让大家第一次了解到这些寄生虫是如何运动的。”他本人未参与这项研究,他的主要工作是研究弓形虫侵入细胞后如何控制免疫系统。
“让人激动的是,我们看到了一些新的分子细节,了解这些寄生虫如何在宿主细胞外发挥作用。这些美丽的结构显示了驱动这种运动的马达如何组装在一起,有望为开发治疗这些疾病的新药打下基础,”Bowler补充说。(生物通 薄荷)
原文检索
pazicky, S., Dhamotharan, K., Kaszuba, K. et al. Structural role of essential light chains in the apicomplexan glideosome. Commun Biol 3, 568 (2020). https://doi.org/10.1038/s42003-020-01283-8